-
摘要:
ABC转运蛋白是具有ATP酶活性并能够跨膜转运底物的膜蛋白超家族。其中,ABCB1、ABCG2、ABCC1与肿瘤多药耐药(MDR)密切相关,是ABC转运蛋白超家族中的研究重点和热点。本文旨在综述ABCB1、ABCG2、ABCC1转运蛋白在肿瘤多药耐药中的最新机制,并探讨靶向抑制这些转运蛋白的最新策略,以期为MDR机制研究及其逆转剂研发提供较系统的参考。
Abstract:The ATP-binding cassette (ABC) transporter superfamily comprises membrane proteins that efflux various substrates across extra- and intracellular membranes. Among them, ABCB1, ABCG2, and ABCC1 are directly linked to tumor multidrug resistance (MDR). This review provides an overview of the current understanding on the novel mechanisms and functions of ABCB1, ABCG2, and ABCC1 transporters in tumor MDR, discusses the latest strategies to target these transporters, and explores further opportunities to overcome MDR.
-
Key words:
- ABC transporter /
- Transmembrane transport /
- MDR /
- Tumor
-
0 引言
多药耐药(multidrug resistance, MDR)是肿瘤化疗失败和复发的主要原因[1],MDR与肿瘤患者不良预后直接相关。ABC(adenosine triphosphate-binding cassette)转运蛋白介导的药物外排增强是MDR的重要机制之一。
人类ABC转运蛋白超家族包括51个成员,根据氨基酸序列及结构特征可分为7个亚家族[2]。大多数ABC转运蛋白由两个ATP结合结构域(NBDs)和两个跨膜结构域(TMDs)组成,见图1A[2]。两个NBD通过结合ATP产生二聚化,水解ATP后两个NBD分离,采取向内开口的构象,使细胞内的底物可以结合在两个TMD之间,然后通过构象变化排除到细胞外[3]。ABC转运蛋白的转运底物包括无机离子、脂肪酸、糖、核苷酸、多肽和药物等[4-5],可以参与线粒体、溶酶体、高尔基体和内质网等细胞器的胞内调节[5],以及膜脂转运、氧化应激防御、解毒和抗原呈递等生物学过程[6]。ABC转运蛋白介导的持续化疗药物外排导致细胞内药物累积浓度降低,从而造成对化疗药物耐药,是产生MDR的重要原因[7]。最新研究表明,至少13个ABC转运蛋白超家族成员与抗肿瘤药物外排和耐药相关[4]。其中,ABCB1,ABCG2和ABCC1三个成员与多种肿瘤的多药耐药关系最为密切,它们的结构和耐药机制研究近几年取得了重大进展[8]。本文旨在重点综述ABCB1、ABCG2、ABCC1增强药物外排导致肿瘤多药耐药的最新分子机制,并初步探讨ABC转运体抑制剂的最新研发策略,以期为克服肿瘤多药耐药提供新见解。
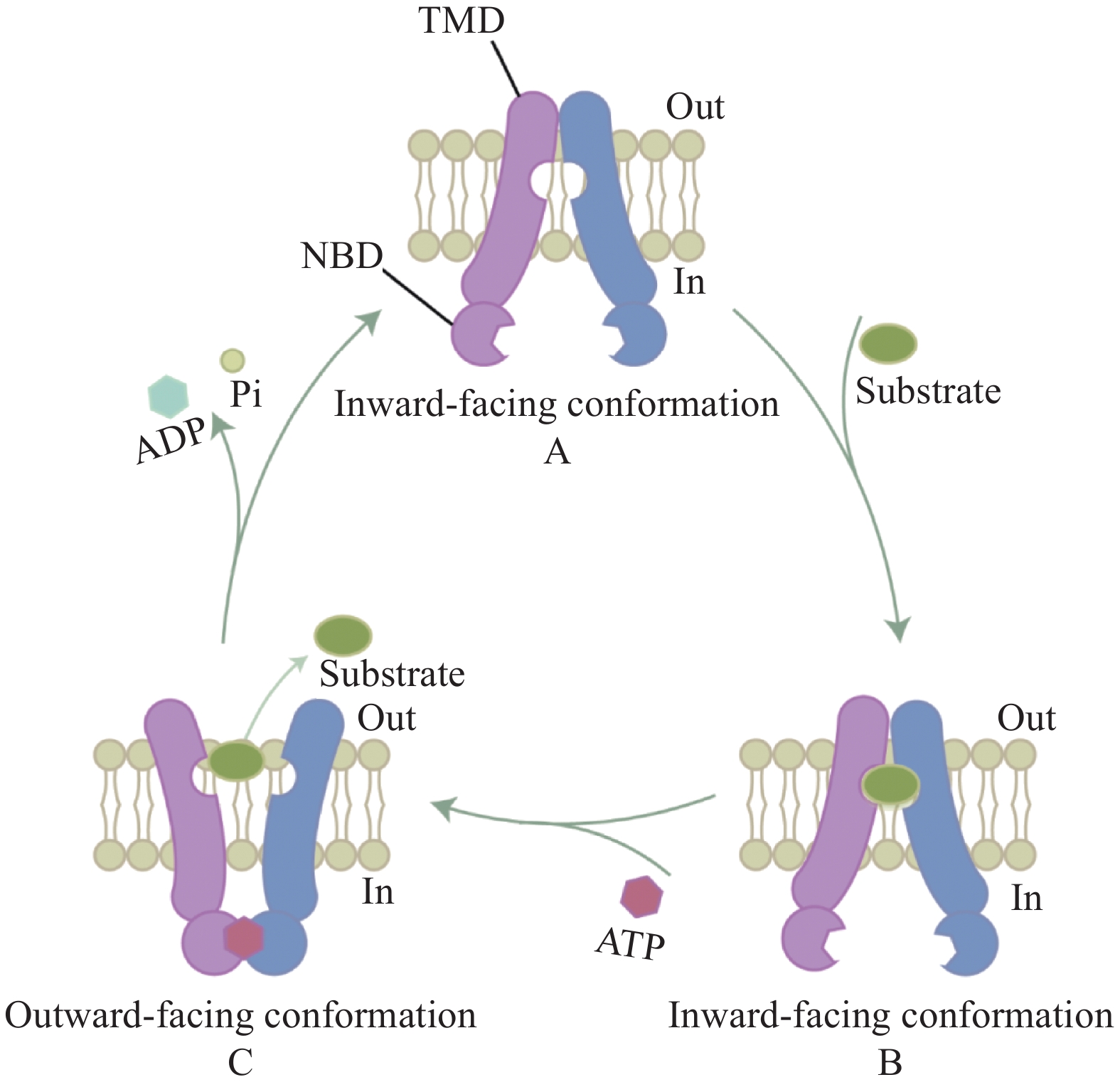
![]() 图 1 ABC转运蛋白的交替访问机制Figure 1 Alternate access mechanisms for ABC transportersA: the ABC transporter comprises two NBDs and two TMDs. In the resting state, ABC transporter exhibits an inward-open conformation; B: ABC transporter-binding substrate; C: conversion of ABC transporter conformation into an outward-open conformation upon ATP binding, resulting in substrate release.
图 1 ABC转运蛋白的交替访问机制Figure 1 Alternate access mechanisms for ABC transportersA: the ABC transporter comprises two NBDs and two TMDs. In the resting state, ABC transporter exhibits an inward-open conformation; B: ABC transporter-binding substrate; C: conversion of ABC transporter conformation into an outward-open conformation upon ATP binding, resulting in substrate release.1 ABC转运蛋白的转运机制
ABC转运蛋白的底物运输,通常会诱发一个经典的“交替访问模型”,见图1[1, 9]。
ABCB1、ABCG2、ABCC1三种蛋白转运底物的机制十分相似,但是存在一些结构细节的差异[1]。具体来讲,ABCB1与ABCG2底物募集来自细胞质和膜间腔,通过“交替访问”机制转运多种底物[10-11]。但是,ABCG2的底物首先与底物结合腔结合,并且随着ATP与NBD结合后移动到低亲和力细胞外腔中,并最终被泵出细胞[11]。而ABCC1的底物只能从细胞质获取而不能从膜内进入,并且仅在具有催化活性的NBD2上发生水解反应[12-13],这种NBD结合ATP的不对称性是ABCC蛋白所特有的。肿瘤细胞正是利用ABC转运蛋白的转运能力将化疗药物转运至细胞外,最终导致多药耐药。
2 ABC转运蛋白介导的多药耐药
2.1 ABC转运蛋白与肿瘤多药耐药
ABCB1在人类约50%的肿瘤中高表达,尤其在未经化疗的肺癌、肝癌、肾癌、直肠癌和结肠癌等癌组织中表达明显增加。在急性淋巴细胞白血病和急性髓性白血病中,化疗药物暴露后也会导致ABCB1表达增加[14]。ABCB1可将多种肿瘤化疗药物如紫杉醇、奥拉帕尼、长春花碱、依托泊苷以及多西他赛转运至细胞外,从而降低其在肿瘤细胞内的浓度[15]。2023年文献报道,具有抗肿瘤活性的强效FLT3抑制剂FN-
1501 也是ABCB1转运的底物,ABCB1过表达的癌细胞对FN-1501 具有耐药性[16]。除了参与药物外排,ABCB1还能够通过抑制肿瘤坏死因子相关的凋亡诱导配体(tumor necrosis factor related apoptosis inducing ligand, TRAIL)所介导的外源凋亡途径和内源凋亡途径来促进肿瘤细胞的生存[17]。Doyle等研究证实ABCG2参与乳腺癌亚群(MCF-7/AdrVp)的多药耐药,因而被命名为乳腺癌耐药蛋白(breast cancer resistance protein, BCRP)[18]。ABCG2介导的肿瘤耐药机制主要包括以下三个方面[19]:(1)ABCG2调控化疗药物的摄取、分散、代谢活性和排泄;(2)肿瘤细胞中ABCG2的高表达直接导致化疗药物的主动外流,包括喜树碱衍生物、黄吡醇、甲氨蝶呤、米托蒽醌及其他结构多样化的化合物,从而引起耐药[20]。(3)ABCG2活性与肿瘤细胞代谢和信号转导通路密切相关,这些代谢和信号转导通路赋予肿瘤耐药性、干细胞性和侵袭性,最终导致不良预后。高表达于肿瘤干细胞表面的ABCG2被认为是肿瘤干细胞特异标志物之一[21],肿瘤干细胞中上调的ABCG2和药物外排可能是肿瘤难治和复发的重要原因。
ABCC1最早被发现影响人肺癌细胞系H69AR对阿霉素的敏感性[22]。后续研究发现,ABCC1调控肿瘤对多种化疗药物的耐药性,包括蒽环类药物(多柔比星和柔红霉素)、依托泊苷、长春新碱、伊立替康/SN-38和甲氨蝶呤等[23]。此外,一些新型的靶向药物也可以通过ABCC1进行转运,包括各种信号转导通路的酪氨酸激酶抑制剂(tailored tyrosine kinase inhibitors, TKIs)[24]。ABCC1在原发性乳腺癌中的表达水平与一线化疗效果呈负相关,与晚期患者不良预后直接相关[23]。
2.2 ABC转运蛋白影响肿瘤多药耐药和肿瘤免疫逃逸的机制
ABC转运蛋白通过转运胆固醇或者多种细胞因子调节肿瘤免疫微环境,从而调控对化疗药物的敏感性[2]。一方面,胆固醇及其衍生物调控单核细胞扩增、中性粒细胞激活、造血干细胞动员和T淋巴细胞增殖影响肿瘤免疫微环境,导致肿瘤耐药[25];另一方面,ABC转运体可以控制细胞内IL-6、CXCL1、CCL5和CCL2等细胞因子的丰度,从而间接调节上皮间充质转化、自噬和DNA损伤修复等,共同降低化疗药物的疗效[26]。
由于ABC转运蛋白自身也受细胞因子的调节,癌症免疫治疗工具可用于靶向ABC转运蛋白以克服肿瘤多药耐药。研究表明,短期TNF-α治疗可以下调结肠癌中ABCB1的表达,而不影响内源性TNF-α水平[27]。由于TNF-α是一种促炎细胞因子,短期治疗可避免持续的下游炎性反应效应。重要的是,短期TNF-α治疗可以抑制NF-κB/p65信号,减少NF-κB与ABCB1启动子的结合,随后下调ABCB1以克服多药耐药[28]。调脂药物联合免疫治疗在肿瘤治疗中的可行性也得到临床前和临床试验验证[29]。
3 靶向ABC转运蛋白克服肿瘤多药耐药的策略
3.1 ABCB1抑制剂
ABCB1的直接抑制剂主要分为三类,一代抑制剂(环孢菌素、他莫昔芬、维拉帕米)因为治疗窗较窄被限制继续开发。二代抑制剂是一代抑制剂的衍生物,如valspodar(PSC 833)、biricodar、emopamil、dexverapamil、gallopamil和Ro11-2933,相对一代抑制剂毒性更低,但与联用的抗癌药物相互作用,导致抗癌药物在血液、肝脏、肾脏中蓄积,引起毒性。相比之下,三代药物,例如Tariquidar(XR9576)、Zosuquidar(LY-335979)、Laniquidar(R101933)、Biricodar(VX-710)等,具有更高的选择性和更强的药效,同时解决1/2代的治疗窗窄、药物相互作用问题,但由于临床结果差异较大,尚未有药物获批[30]。
此外,研究还发现一些天然化合物,如生物碱类(pervilleine F)、香豆素类(cnidiadin)、黄酮类化合物(桔皮素、黄芩素、槲皮素)和二萜类(浆果赤霉素Ⅲ、紫杉醇苷D)等可以作为ABCB1转运蛋白抑制剂,因此又被称为第四代ABCB1抑制剂[31]。将这些天然化合物与化疗药物联用,已经取得明显效果,例如,Guajadial作为一种天然的巯基萜类化合物,在MCF-7/ADR和MCF-7/PTX耐药细胞中与紫杉醇和阿霉素联用,通过抑制ABCB1和ABCG2使紫杉醇和阿霉素增敏[32],姜黄素和维生素D3与紫杉醇联合治疗可抑制乳腺癌中ABCB1的表达,增强药物的敏感性[33],在A549/T荷瘤裸鼠模型中,人参皂苷Rg5联合多西紫杉醇(TXT)治疗较相同剂量TXT单独治疗显著抑制耐药肿瘤的生长,且不增加毒性[34]。
由于直接抑制ABCB1的药物选择性差以及导致组织损伤,因此研究者们将靶点转移至调控ABCB1蛋白表达的通路。前期研究表明,Hippo信号通路可以通过调节ABCB1来影响肝细胞癌中的瑞戈非尼耐药[35]。Hedgehog通路抑制剂HhAntag691显著抑制ABCB1的表达[36]。在此基础上,最新研究发现,雷公藤甲素是一种强效的Hedgehog抑制剂,可通过阻断Hedgehog通路影响ABCB1表达最终逆转非小细胞肺癌对紫杉醇的耐药[37]。此外,ROR1蛋白被发现在化药耐药的乳腺癌细胞中过表达,通过MAPK/ERK和p53调节ABCB1的表达以及稳定性[38]。加入RORγ抑制剂SR2211后,Docetaxel和Cabazitaxel耐药的前列腺癌细胞对两种药物敏感性提高[39]。
3.2 ABCG2抑制剂
1998年,Rabindran等首次发现烟曲霉菌产生的真菌毒素(fumitremorgin C, FTC)是ABCG2的功能性抑制剂[40]。随后,他们在此基础上开发了许多高效的ABCG2抑制剂,如FTC的衍生物Ko143是最有效的ABCG2功能抑制剂之一,并且具有较低的细胞毒性。Ko143在较高浓度下也可以抑制ABCB1和ABCC1介导的底物运输[41]。通过药物再利用方法还确定了钙通道阻滞剂、抗HIV和黄嘌呤氧化酶抑制剂等多种可再利用的ABCG2抑制剂[42]。近年来,甲磺酸伊马替尼被证明是ABCG2转运蛋白的有效抑制剂,可在体外逆转托泊替康和 SN-38 的耐药性[30],类黄酮单体作为另一种ABCG2的有效、无毒和选择性调节剂可以显著增加细胞内拓扑替康和米托蒽醌水平[43]。此外,由Scandion Oncology A/S开发的口服药物SCO-101是一种靶向ABCG2、UGT1A1和SRPK1的抑制剂,二期临床实验证明SCO-101联合亚叶酸、氟尿嘧啶和伊立替康为没有其他积极治疗选择的大量经治转移性结直肠癌(metastatic colorectal cancer, mCRC)患者提供了具有临床意义的总生存期获益[44]。研究还发现了一种潜在的双靶点抑制剂Y22,通过阻断ABCB1和ABCG2的外排功能来逆转MDR[45]。因此,Y22与常用化疗药物联合应用可能具有临床疗效。
3.3 ABCC1抑制剂
过去一些有机阴离子转运体抑制剂(如吲哚美辛和亚砜吡啶酮)以及一些非甾体抗炎药(如舒林酸、布洛芬和托美汀等)作为ABCC1的抑制剂用于临床试验,然而引起非特异性影响以及不明确的抗肿瘤作用逐渐被取代[23]。目前最常见的ABCC1抑制剂是半胱氨酸白三烯受体1拮抗剂(MK-571)[46],大量实验证明MK-571竞争性地抑制ABCC1的有机阴离子运输并逆转ABCC1介导的细胞内多药耐药现象。然而,MK-571同样能有效地抑制其他半胱氨酸白三烯受体拮抗剂,例如LY171883和BAY-u9773[47],这样会导致难以预期的不良反应。目前存在一些天然化合物,如agosterol A和几种黄酮类化合物(包括芹菜素、山奈酚、槲皮素、柚皮素、杨梅素和染料木素)可以作为ABCC1转运蛋白的调节剂[23]。除了对ABCC1表现出抑制活性,黄酮类化合物还可以刺激ABCC1的ATP酶活性以及ABCC1转运谷胱甘肽[48]。尽管目前仍在进行更有效抑制ABCC1活性的类黄酮衍生物研究,但黄酮类化合物多样的活性对于其作为潜在临床ABCC1抑制剂提出了挑战。后来,HSP90抑制剂AUY922被首次证明了可以使ABCB1和ABCC1的显著降低维持长达8日,因此将AUY922与目前常用的细胞毒性药物联合使用可以防止传统细胞毒性药物治疗导致的转移和耐药等不良反应[49]。同年,Gao等证明IRE1α的RNA酶抑制剂4μ8C可以抑制抗癌药物5-氟尿嘧啶、卡培他滨和奥沙利铂对ABCB1、ABCC1、ABCG2等转运蛋白的诱导表达,进而增强细胞毒性药物对耐药的结肠癌细胞的治疗效果[50]。随着ABCC1结构研究的进一步深入,基于冷冻电镜研究,2023年报道了一种名为CPI1的大环肽可以与ABCC1结合阻止ATP水解和底物转运所必需的构象变化,进而显著抑制ABCC1的转运能力[51]。
3.4 纳米给药载体在克服MDR中的作用
尽管ABC转运蛋白抑制剂的发现促进了肿瘤多药耐药的缓解,但由于缺乏特异性、生物利用度缩短、不良反应和剂量优化相关问题以及与其他化疗药物相互作用等因素,抑制剂的使用受到限制。纳米载体是新兴的纳米级药物递送系统,其核心可以是脂质体,也可以是多聚体聚乳酸-羟基乙酸共聚物(PLGA)或者聚苯乙烯等。纳米载体的使用增强了药物生物有效性和靶向特异性[52]。研究报道多肽纳米颗粒(PNP)可递送两个siRNA(分别靶向沉默TGFβ和Cox2)。在原位肝细胞癌小鼠中,通过静脉注射系统性给药将siRNA递送到肝脏中,能够显著减少肿瘤,还可与PD-L1单克隆抗体联合使用,进一步增强治疗效果[53]。此外,研究人员还设计出一种自催化原位组装的纳米颗粒。合成的酪氨酸(Tyr)修饰的肽包封的碘(I)掺杂CuS纳米粒子(CuS-I@P1 NPs)作为自催化的构建模块,通过纳米粒子自身催化的Tyr-Tyr缩合反应在肿瘤细胞内自行组装[54]。这种纳米颗粒具有制备方便、反应特异性高、生物相容性好等优点,为靶点特异性肿瘤治疗提供了一种可推广的新策略。
4 结论与展望
ABC转运蛋白介导产生的肿瘤多药耐药是化疗策略失败最常见的原因之一,ABCB1、ABCG2、ABCC1是导致肿瘤多药耐药的重要蛋白质。以上研究表明,这些转运体的小分子抑制剂可以增强肿瘤患者对化疗药物的敏感性,大量的基础研究和临床研究正在进行中。然而,在临床实践中仍然面临巨大挑战,如ABCB1抑制剂未能明显改善患者预后,目前也还没有ABC转运蛋白抑制剂与化疗药物联用成功的例子。对ABC转运蛋白介导的多药耐药机制还需进行深入研究,包括药物分子的特异性,多种ABC转运蛋白在细胞内的补偿机制等。不同的ABC转运蛋白具有相似的药物转运机制,但也有一些独特的分子细节和结构基础。转运的药物有一些特性,也有一些共性,其背后的分子细节和结构基础仍有待进一步研究。近期我们课题组用冷冻电镜解析了非对称ATP结合诱导ABC转运体构象变化的结构基础,揭示了ABC转运蛋白特异性识别和转运药物的分子机制,而且还提出了所有多药耐药相关蛋白(MRPs)共同的底物结合模式,进一步拓宽了我们对多药耐药分子机制的了解[3,55]。下一步,开发出特异性更好、毒性更小的的靶向ABC转运蛋白的药物也将有望在临床实践中取得突破。此外,中药具有多靶点、多环节的作用特点,作为天然产物不良反应相对较小,将其作为药物转运抑制剂逆转肿瘤MDR可能具有优势[34],中药与化疗药物联合使用逆转肿瘤MDR的作用机制值得深入探究。此外,纳米颗粒因其靶点特异性引起人们的关注,其在生物系统中的靶向组装为克服肿瘤多药耐药带来了巨大的希望。
Competing interests: The authors declare that they have no competing interests.利益冲突声明:所有作者均声明不存在利益冲突。作者贡献:邢小珂:文章撰写与修改王淑贤、李娟娟:文章校对宋启斌、张平锋:文章构思与修改 -
[1] Baril SA, Gose T, Schuetz JD. How Cryo-EM has expanded our understanding of membrane transporters[J]. Drug Metab Dispos, 2023, 51(8): 904-922. doi: 10.1124/dmd.122.001004
[2] Fan J, To KKW, Chen ZS, et al. ABC transporters affects tumor immune microenvironment to regulate cancer immunotherapy and multidrug resistance[J]. Drug Resistance Updates, 2023, 66: 100905. doi: 10.1016/j.drup.2022.100905
[3] Bloch M, Raj I, Pape T, et al. Structural and mechanistic basis of substrate transport by the multidrug transporter mrp4[J]. Structure, 2023, 31(11): 1407-1418. e6.
[4] Duvivier L, Gerard L, Diaz A, et al. Linking ABC transporters to the hallmarks of cancer[J]. Trends Cancer, 2024, 10(2): 124-134. doi: 10.1016/j.trecan.2023.09.013
[5] Villa M, Wu J, Hansen S, et al. Emerging role of ABC transporters in glia cells in health and diseases of the central nervous system[J]. Cells, 2024, 13(9): 740. doi: 10.3390/cells13090740
[6] Bodó A, Bakos E, Szeri F, et al. The role of multidrug transporters in drug availability, metabolism and toxicity[J]. Toxicol Lett, 2003, 140-141: 133-143. doi: 10.1016/S0378-4274(02)00497-6
[7] Pote MS, Gacche RN. ATP-binding cassette efflux transporters and MDR in cancer[J]. Drug Discov Today, 2023, 28(5): 103537. doi: 10.1016/j.drudis.2023.103537
[8] Mohammad IS, He W, Yin L. Understanding of human ATP binding cassette superfamily and novel multidrug resistance modulators to overcome MDR[J]. Biomed Pharmacother, 2018, 100: 335-348. doi: 10.1016/j.biopha.2018.02.038
[9] Locher KP. Mechanistic diversity in ATP-binding cassette (ABC) transporters[J]. Nat Struct Mol Biol, 2016, 23(6): 487-493. doi: 10.1038/nsmb.3216
[10] Gewering T, Waghray D, Parey K, et al. Tracing the substrate translocation mechanism in P-glycoprotein[J]. ELife, 2024, 12: RP90174. doi: 10.7554/eLife.90174.3
[11] Kowal J, Ni D, Jackson SM, et al. Structural basis of drug recognition by the multidrug transporter ABCG2[J]. J Mol Biol, 2021, 433(13): 166980. doi: 10.1016/j.jmb.2021.166980
[12] Wang L, Johnson ZL, Wasserman MR, et al. Characterization of the kinetic cycle of an ABC transporter by single-molecule and cryo-EM analyses[J]. ELife, 2020, 9: e56451. doi: 10.7554/eLife.56451
[13] Johnson ZL, Chen J. Structural basis of substrate recognition by the multidrug resistance protein MRP1[J]. Cell, 2017, 168(6): 1075-1085. e9.
[14] Wang X, Zhang H, Chen X. Drug resistance and combating drug resistance in cancer[J]. Cancer Drug Resist, 2019, 2(2): 141-160.
[15] Haider T, Pandey V, Banjare N, et al. Drug resistance in cancer: Mechanisms and tackling strategies[J]. Pharmacol Rep, 2020, 72(5): 1125-1151. doi: 10.1007/s43440-020-00138-7
[16] Zhang M, Huang MN, Dong XD, et al. Overexpression of ABCB1 confers resistance to FLT3 inhibitor FN-1501 in cancer cells: In vitro and in vivo characterization[J]. Am J Cancer Res, 2023, 13(12): 6026-6037.
[17] Souza PS, Madigan JP, Gillet JP, et al. Expression of the multidrug transporter P-glycoprotein is inversely related to that of apoptosis-associated endogenous TRAIL[J]. Exp Cell Res, 2015, 336(2): 318-328. doi: 10.1016/j.yexcr.2015.06.005
[18] Doyle LA, Yang W, Abruzzo LV, et al. A multidrug resistance transporter from human MCF-7 breast cancer cells[J]. Proc Natl Acad Sci U S A, 1998, 95(26): 15665-15670. doi: 10.1073/pnas.95.26.15665
[19] Ross DD, Nakanishi T. Impact of breast cancer resistance protein on cancer treatment outcomes[J]. Methods Mol Biol, 2010, 596: 251-290.
[20] Doyle LA, Ross DD. Multidrug resistance mediated by the breast cancer resistance protein BCRP (ABCG2)[J]. Oncogene, 2003, 22(47): 7340-7358. doi: 10.1038/sj.onc.1206938
[21] Zhang L, Zhao J, Liang C, et al. A novel biosensor based on intestinal 3D organoids for detecting the function of BCRP[J]. Drug Deliv, 2017, 24(1): 1453-1459. doi: 10.1080/10717544.2017.1381199
[22] Cole SP, Bhardwaj G, Gerlach JH, et al. Overexpression of a transporter gene in a multidrug-resistant human lung cancer cell line[J]. Science, 1992, 258(5088): 1650-1654. doi: 10.1126/science.1360704
[23] Hanssen KM, Haber M, Fletcher JI. Targeting multidrug resistance-associated protein 1 (MRP1)-expressing cancers: Beyond pharmacological inhibition[J]. Drug Resist Updat, 2021, 59: 100795. doi: 10.1016/j.drup.2021.100795
[24] Gelbmann CB, Kalejta RF. The membrane-spanning peptide and acidic cluster dileucine sorting motif of UL138 are required to downregulate MRPl drug transporter function in human cytomegalo virus-infected cells[J]. J Virol, 2019, 93(11): e00430-19.
[25] Chaves-Filho AB, Schulze A. Cholesterol atlas of tumor microenvironment provides route to improved CAR-T therapy[J]. Cancer Cell, 2023, 41(7): 1204-1206. doi: 10.1016/j.ccell.2023.05.013
[26] Erin N, Grahovac J, Brozovic A, et al. Tumor microenvironment and epithelial mesenchymal transition as targets to overcome tumor multidrug resistance[J]. Drug Resist Updat, 2020, 53: 100715. doi: 10.1016/j.drup.2020.100715
[27] Kyle-Cezar F, Echevarria-Lima J, Rumjanek VM. Independent regulation of ABCB1 and ABCC activities in thymocytes and bone marrow mononuclear cells during aging[J]. Scand J Immunol, 2007, 66(2-3): 238-248. doi: 10.1111/j.1365-3083.2007.01965.x
[28] Walther W, Kobelt D, Bauer L, et al. Chemosensitization by diverging modulation by short-term and long-term TNF-α action on ABCB1 expression and NF-κb signaling in colon cancer[J]. Int J Oncol, 2015, 47(6): 2276-2285. doi: 10.3892/ijo.2015.3189
[29] Zheng M, Zhang W, Chen X, et al. The impact of lipids on the cancer-immunity cycle and strategies for modulating lipid metabolism to improve cancer immunotherapy[J]. Acta Pharm Sin B, 2023, 13(4): 1488-1497. doi: 10.1016/j.apsb.2022.10.027
[30] Duan C, Yu M, Xu J, et al. Overcoming cancer multi-drug resistance (MDR): Reasons, mechanisms, nanotherapeutic solutions, and challenges[J]. Biomed Pharmacother, 2023, 162: 114643. doi: 10.1016/j.biopha.2023.114643
[31] Karthikeyan S, Hoti SL. Development of fourth generation ABC inhibitors from natural products: A novel approach to overcome cancer multidrug resistance[J]. Anticancer Agents Med Chem, 2015, 15(5): 605-615. doi: 10.2174/1871520615666150113103439
[32] Li Y, Zhai Z, Li H, et al. Guajadial reverses multidrug resistance by inhibiting abc transporter expression and suppressing the PI3K/Akt pathway in drug-resistant breast cancer cells[J]. Chem Biol Interact, 2019, 305: 98-104. doi: 10.1016/j.cbi.2019.03.032
[33] Attia YM, El-Kersh DM, Ammar RA, et al. Inhibition of aldehyde dehydrogenase-1 and p-glycoprotein-mediated multidrug resistance by curcumin and vitamin D3 increases sensitivity to paclitaxel in breast cancer[J]. Chem Biol Interact, 2020, 315: 108865. doi: 10.1016/j.cbi.2019.108865
[34] Feng SL, Luo HB, Cai L, et al. Ginsenoside Rg5 overcomes chemotherapeutic multidrug resistance mediated by abcb1 transporter: In vitro and in vivo study[J]. J Ginseng Res, 2020, 44(2): 247-257. doi: 10.1016/j.jgr.2018.10.007
[35] Suemura S, Kodama T, Myojin Y, et al. CRISPR loss-of-function screen identifies the hippo signaling pathway as the mediator of regorafenib efficacy in hepatocellular carcinoma[J]. Cancers(Basel), 2019, 11(9): 1362.
[36] Zhang Y, Laterra J, Pomper MG. Hedgehog pathway inhibitor HhAntag691 is a potent inhibitor of ABCG2/BCRP and ABCB1/PGP[J]. Neoplasia, 2009, 11(1): 96-101. doi: 10.1593/neo.81264
[37] Li LB, Yang LX, Liu L, et al. Targeted inhibition of the HNF1A/SHH axis by triptolide overcomes paclitaxel resistance in non-small cell lung cancer[J]. Acta Pharmacol Sin, 2024, 45(5): 1060-1076.
[38] Fultang N, Illendula A, Lin J, et al. ROR1 regulates chemoresistance in breast cancer via modulation of drug efflux pump ABCB1[J]. Sci Rep, 2020, 10(1): 1821. doi: 10.1038/s41598-020-58864-0
[39] Wang Y, Huang Z, Chen CZ, et al. Therapeutic targeting of MDR1 expression by RORγ antagonists resensitizes cross-resistant crpc to taxane via coordinated induction of cell death programs[J]. Mol Cancer Ther, 2020, 19(2): 364-374. doi: 10.1158/1535-7163.MCT-19-0327
[40] Rabindran SK, He H, Singh M, et al. Reversal of a novel multidrug resistance mechanism in human colon carcinoma cells by fumitremorgin C[J]. Cancer Research, 1998, 58(24): 5850-5858.
[41] Weidner LD, Zoghbi SS, Lu S, et al. The inhibitor Ko143 is not specific for ABCG2[J]. J Pharmacol Exp Ther, 2015, 354(3): 384-393. doi: 10.1124/jpet.115.225482
[42] Zattoni IF, Delabio LC, Dutra JP, et al. Targeting breast cancer resistance protein (BCRP/ABCG2): Functional inhibitors and expression modulators[J]. Eur J Med Chem, 2022, 237: 114346. doi: 10.1016/j.ejmech.2022.114346
[43] Wong ILK, Zhu X, Chan KF, et al. Flavonoid monomers as potent, nontoxic, and selective modulators of the breast cancer resistance protein (ABCG2)[J]. J Med Chem, 2021, 64(19): 14311-14331. doi: 10.1021/acs.jmedchem.1c00779
[44] Bergmann TK, Stage TB, Stenvang J, et al. Four phase 1 trials to evaluate the safety and pharmacokinetic profile of single and repeated dosing of SCO-101 in adult male and female volunteers[J]. Basic Clin Pharmacol Toxicol, 2020, 127(4): 329-337. doi: 10.1111/bcpt.13466
[45] Li H, Zhang SL, Jia YH, et al. Imidazo[1, 2-a]pyridine derivatives as novel dual-target inhibitors of ABCB1 and ABCG2 for reversing multidrug resistance[J]. J Med Chem, 2023, 66(4): 2804-2831. doi: 10.1021/acs.jmedchem.2c01862
[46] Gekeler V, Ise W, Sanders KH, et al. The leukotriene LTD4 receptor antagonist MK571 specifically modulates MRP associated multidrug resistance[J]. Biochem Biophys Res Commun, 1995, 208(1): 345-352. doi: 10.1006/bbrc.1995.1344
[47] Csandl MA, Conseil G, Cole SPC. Cysteinyl leukotriene receptor 1/2 antagonists nonselectively modulate organic anion transport by multidrug resistance proteins (mrp 1-4)[J]. Drug Metab Dispos, 2016, 44(6): 857-866.
[48] Cole SPC. Targeting multidrug resistance protein 1 (MRP1, ABCC1): Past, present, and future[J]. Annu Rev of Pharmacol Toxicol, 2014, 54: 95-117. doi: 10.1146/annurev-pharmtox-011613-135959
[49] Bacon NA, Larre I, Lawag AA, et al. Low dose HSP90 inhibition with AUY922 blunts rapid evolution of metastatic and drug resistant phenotypes induced by TGF-β and paclitaxel in A549 cells[J]. Biomed Pharmacother, 2020, 129: 110434. doi: 10.1016/j.biopha.2020.110434
[50] Gao Q, Li XX, Xu YM, et al. IRE1α-targeting downregulates ABC transporters and overcomes drug resistance of colon cancer cells[J]. Cancer Lett, 2020, 476: 67-74. doi: 10.1016/j.canlet.2020.02.007
[51] Pietz HL, Abbas A, Johnson ZL, et al. A macrocyclic peptide inhibitor traps MRP1 in a catalytically incompetent conformation[J]. Proc Natl Acad Sci U S A, 2023, 120(11): e2220012120. doi: 10.1073/pnas.2220012120
[52] Boehnke N, Straehla JP, Safford HC, et al. Massively parallel pooled screening reveals genomic determinants of nanoparticle delivery[J]. Science, 2022, 377(6604): eabm5551. doi: 10.1126/science.abm5551
[53] Kim W, Ye Z, Simonenko V, et al. Codelivery of TGFβ and Cox2 siRNA inhibits HCC by promoting T-cell penetration into the tumor and improves response to immune Checkpoint Inhibitors[J]. NAR Cancer, 2024, 6(1): zcad059. doi: 10.1093/narcan/zcad059
[54] Chen J, Liu Y, Chen F, et al. Non-Faradaic optoelectrodes for safe electrical neuromodulation[J]. Nat Commun, 2024, 15(1): 405. doi: 10.1038/s41467-023-44635-8
[55] Wang J, Li X, Wang F-F, et al. Placing steroid hormones within the human ABCC3 transporter reveals a compatible amphiphilic substrate-binding pocket[J]. EMBO J, 2023, 42(17): e113415. doi: 10.15252/embj.2022113415



 下载:
下载:

