Effects of Lentivirus-Mediated CIB1 Silencing on Biological Behavior of Breast Cancer Cells
-
摘要:目的
探讨CIB1对三阴性乳腺癌细胞增殖、迁移、凋亡和侵袭的影响及作用机制。
方法将MDA-MB-231和MDA-MB-468细胞分为CIB1敲低组(感染CRISPR/Cas9慢病毒)和阴性对照组。采用CCK-8和EdU实验检测各组细胞增殖,流式细胞术测定细胞凋亡,划痕实验和Transwell实验检测细胞迁移及侵袭。采用qRT-PCR和Western blot检测细胞内β-连环蛋白(β-Catenin)、活化蛋白C(APC)、糖原合酶激酶3β(GSK-3β)、c-myc的mRNA和蛋白表达水平。
结果与阴性对照组比较,CIB1敲低组增殖、侵袭和迁移细胞数减少(P<0.05),凋亡细胞数增加(P<0.05),β-Catenin、APC、c-myc的mRNA和蛋白表达量降低(P<0.05),GSK-3β的mRNA和蛋白表达量增高(P<0.05)。
结论敲低CIB1可抑制乳腺癌细胞增殖、迁移及侵袭,促进细胞凋亡,其机制可能与抑制Wnt/β-Catenin信号通路有关。
Abstract:ObjectiveTo investigate the effects of calcium and integrin-binding protein 1 (CIB1) on the cell proliferation, invasion, apoptosis, and migration of triple-negative breast cancer cells and its possible mechanism.
MethodsMDA-MB-231 and MDA-MB-468 cells were divided into CIB1-knockdown(infected with CRISPR/Cas9 lentivirus) and negative-control groups. Cell Counting Kit-8 (CCK-8) and 5-ethynyl-2′-deoxyuridine (EdU) assays were performed to detect cell proliferation. Cell apoptosis was determined through flow cytometry. Scratch and Transwell experiments were conducted to measure the migration and invasion abilities of cells. The mRNA and protein expression levels of β-catenin, adenomatous polyposis coli (APC), glycogen synthase kinase 3β (GSK-3β), and c-myc were detected via real-time quantitative polymerase chain reaction and Western blot.
ResultsCompared with the negative-control group, the CIB1-knockdown group showed decreased cell proliferation, invasion, and migration (P<0.05) and increased cell apoptosis (P<0.05). The mRNA and protein expressions of β-catenin, APC, and c-myc decreased (P<0.05), and that of GSK-3β increased (P<0.05).
ConclusionCIB1 knockdown can inhibit cell proliferation, invasion, and migration and promote the apoptosis of breast cancer cells. Its mechanism may be related to the inhibition of Wnt/β-catenin signaling pathway.
-
Key words:
- CIB1 /
- Triple negative breast cancer /
- Proliferation /
- Migration /
- Invasion /
- Wnt/β-catenin signaling pathway
-
0 引言
乳腺癌是一种常见的恶性肿瘤,2022年全球女性新发病例估计为231万,占全球所有癌症病例的11.6%,死亡人数占全部癌症死亡人数的6.9%[1]。传统乳腺癌的治疗方法包括手术、放疗、化疗、激素治疗和免疫治疗,往往不能解决由乳腺癌亚型的复杂性和异质性所导致的耐药和转移,因此,需要探索新的有效的乳腺癌治疗靶点。随着基因组学和基因编辑技术的发展,基因靶向治疗在乳腺癌治疗中越来越受到关注。研究表明,许多基因都参与了乳腺癌的发生发展过程,包括细胞周期蛋白D1、基质金属蛋白酶、E-钙黏蛋白和钙整合素结合蛋白1(calcium and integrin-binding protein 1,CIB1),其中CIB1与乳腺癌不良预后有关[2]。CIB1是恶性肿瘤的潜在关键介质,也是复杂的致癌信号通路网络的关键汇聚点。有研究表明CIB1基因在多种类型的肿瘤细胞中显著过表达,并与肿瘤的发生、增殖、侵袭和转移有关[3],敲减三阴乳腺癌(triple-negative breast cancer,TNBC)中CIB1,可抑制TNBC细胞的存活和增殖,显著缩小肿瘤体积[4]。Wnt/β-catenin信号通路是细胞内最重要的信号转导通路之一,影响下游多种效应分子的激活状态,与多种人类肿瘤的发展密切相关,在乳腺癌细胞的增殖和侵袭中起着重要作用[5]。然而,在乳腺癌中,Wnt/β-catenin信号通路被CIB1激活的机制尚无明确报道。本研究通过探索敲低CIB1在乳腺癌MDA-MB-231和MDA-MB-468细胞的增殖、迁移、侵袭和凋亡中的作用,进一步确定其作用机制,为乳腺癌基因靶向治疗提供新的思路。
1 材料与方法
1.1 实验材料
MDA-MB-231细胞和MDA-MB-468细胞(上海誉驰生物);胎牛血清(美国Gibco公司);CRISPR/Cas9慢病毒载体及对照空载体慢病毒购于上海吉凯基因公司;CCK-8细胞增殖试剂盒(苏州优逸兰迪生物科技有限公司);Annexin V-PE/7AAD凋亡检测试剂盒(美国BD公司);Matrigel基质胶(美国Corning公司);CIB1、β-Catenin、GSK-3β、c-myc抗体(美国Proteintech公司);p-GSK-3β(Ser9)、APC抗体(英国Abcam公司);ECL化学发光底物(北京兰杰柯科有限公司);生物安全柜(美国Thermo Fisher Scientific公司)。
1.2 实验方法
1.2.1 生物信息学分析
通过癌症基因组图库(The Cancer Genome Atlas,TCGA)共筛选出
1101 例乳腺癌组织和113例癌旁组织样本,比较两组CIB1的表达情况。1.2.2 乳腺癌细胞培养及慢病毒感染细胞构建
使用90% DMEM高糖培养基、10%胎牛血清配制完全培养基来培养乳腺癌MDA-MB-231和MDA-MB-468细胞,将细胞置于37℃、5%CO2的培养箱内培养。取对数生长期细胞平铺于12孔板,分别感染阴性对照慢病毒( NC组)以及CRISPR/Cas9慢病毒(CIB1-KD组),以细胞的病毒感染复数(multiplicity of infection,MOI)为20计算需要加入的病毒体积,感染12~16 h后更换成完全培养基,72 h后荧光显微镜观察感染效率。Western blot实验检测各组内CIB1的蛋白相对表达,确认感染情况。
1.2.3 CCK-8实验
取对数生长期细胞,于96孔板内每孔铺5×103个细胞,待细胞贴壁后每孔加入10 μl CCK-8溶液,于培养箱内孵育2 h后使用酶标仪测定450 nm的OD值,分别记录0、24、48、72 h的OD值。
1.2.4 EdU实验
取对数生长期细胞,于96孔板内每孔铺7×103个细胞,贴壁后每孔加入100 μl配制好的EdU培养基,培养箱内孵育2 h,按照说明书进行细胞固定、Apollo染色、DNA染色等操作,荧光显微镜拍照记录。
1.2.5 流式细胞术检测细胞凋亡
收集对数生长期细胞,消化后用预冷的PBS溶液清洗2次,并用1×Binding Buffer重悬细胞,根据说明书进行参数调节。每管加入5 μl Annexin V和5 μl 7-AAD染料进行染色,避光、静置15 min后上机,于1 h内进行检测。
1.2.6 Transwell侵袭实验
提前将Matrigel胶铺在24孔板的小室内,培养箱内孵育6 h,取对数生长期的细胞,于上室加入含5%FBS的DMEM高糖培养基,下室加入含20%FBS的DMEM高糖培养基,培养36 h后终止实验。采用4%多聚甲醛进行细胞固定、结晶紫染色,用PBS清洗,显微镜拍照,并使用Image J软件进行细胞计数。
1.2.7 划痕实验检测细胞迁移
于6孔板背面使用记号笔进行划线,取对数生长期细胞进行6孔板铺板,待细胞贴壁后加入不含FBS的DMEM高糖培养基,随后在6孔板内使用200 μl黄枪头垂直进行划线,继续用不含FBS的DMEM高糖培养基进行培养,0 h和48 h时显微镜下观察并拍照各组细胞划痕愈合状态,使用Image J软件分析划痕面积并计算划痕愈合率。
1.2.8 qRT-PCR实验检测mRNA表达
当细胞密度为90%左右时提取各组细胞的RNA,进行浓度测定,并按照说明书将RNA反转录为cDNA,以GAPDH为内参,随后进行扩增实验来测定Wnt/β-Catenin通路关键因子的mRNA相对表达。设置反应条件为95℃预变性10 s;90℃变性5 s、60℃退火20 s,循环40次;最后95℃ 60 s、55℃ 60 s、95℃ 30 s延伸。引物序列见表1。
表 1 引物序列Table 1 Primer sequencesGene name Sequence(5′→3′) β-catenin CCAGGTGGTGGTTAATAAGGCT CTCACGATGATGGGAAAGGTTA APC AGGCTGACAAGTCATCTGGGAAC CAGGCTGTGAGTGAATGATGTTG GSK-3β GTTAGCAGAGACAAGGACGGCA GCAATACTTTCTTGATGGCGAC c-myc GGTCTTCCCCTACCCTCTCAAC GCTGTGAGGAGGTTTGCTGTG GAPDH GGAAGCTTGTCATCAATGGAAATC TGATGACCCTTTTGGCTCCC 1.2.9 Western blot实验检测蛋白表达
待细胞密度为80%~90%左右时,使用配制好的RIPA裂解液裂解细胞并提取各组细胞的蛋白,使用SDS-PAGE凝胶试剂盒配胶,经过电泳、电转、封闭、洗膜、孵育一抗(4℃孵育过夜)、洗膜、孵育二抗、洗膜、曝光等一系列操作,使用Image J软件进行条带灰度分析,计算蛋白相对表达量。抗体稀释:β-Catenin多克隆抗体(1:
1000 );APC多克隆抗体(1:1000 );GSK-3β多克隆抗体(1:1000 );p-GSK-3β(Ser9)单克隆抗体(1:10000 );c-myc单克隆抗体(1:10000 );GAPDH单克隆抗体(1:1000 );辣根过氧化物酶山羊抗兔IgG(1:3000 );辣根过氧化物酶山羊抗小鼠IgG(1:5000 )。1.3 统计学方法
采用Graphpad 8.0软件进行统计分析及绘图,两组间比较若符合正态分布采用t检验,不符合正态分布的采用Mann-Whitney U检验,多组间比较采用单因素方差分析(One-way ANOVA),两两比较采用LSD法,CCK-8实验三个不同时间的结果采用两因素方差分析,P<0.05认为差异具有统计学意义。
2 结果
2.1 CIB1在乳腺癌及癌旁组织中的表达
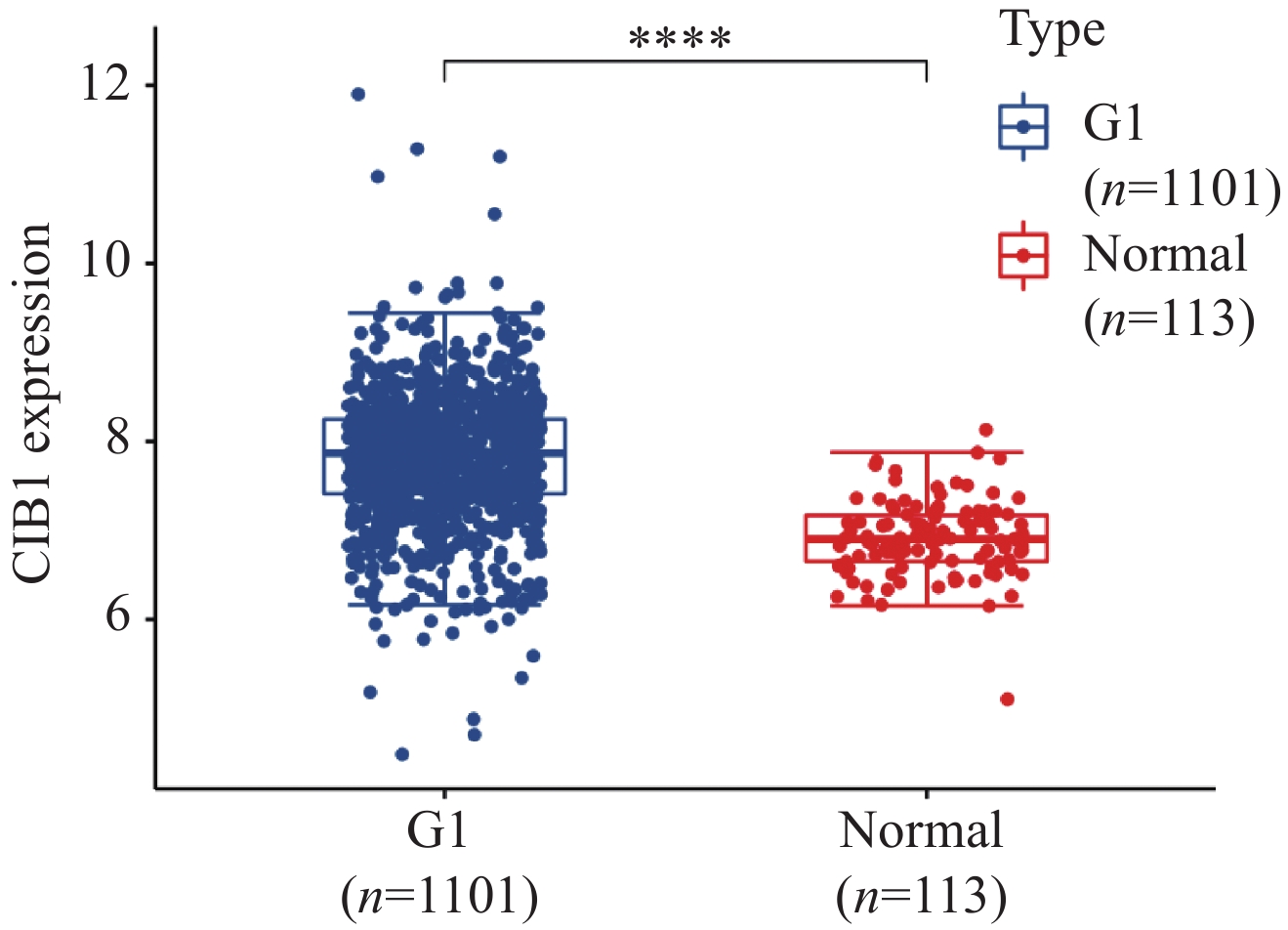
TCGA数据库分析显示,CIB1在乳腺癌组织的表达量高于癌旁组织,差异具有统计学意义(P<
0.0001 ),见图1。2.2 慢病毒感染乳腺癌细胞效率验证
根据不同的敲低位点,sgRNA共分为三种,即
11445 、11446 、11447 ,慢病毒感染成功后提取细胞DNA进行测序。正确连接的重组载体测序结果表明,在MDA-MB-231细胞中,只有11445 、11447 两组靶点序列分别显示为GATTCGCTCCTTGAAGGGGT和GCCAAAGACAGCCTTAGCTT(红色框内),显示插入片段序列与设计合成编码序列完全一致,说明sgRNA成功插在正确位点,见图2。进一步通过Western blot实验检测两株细胞株内CIB1的蛋白表达情况,结果显示CIB1-KD(11447 )组CIB1蛋白表达量低于NC组,说明已成功构建CIB1-KD的MDA-MB-231细胞,差异具有统计学意义(P<0.0001 ),见图3A~B。随后,根据MDA-MB-231细胞的感染结果,我们选取11447 重组载体病毒感染MDA-MB-468细胞,同时感染阴性对照病毒作为对照组,Western blot实验结果显示CIB1敲低组(CIB1-KD)内CIB1的相对蛋白表达低于NC组(P<0.05),说明敲低CIB1的MDA-MB-468细胞模型构建成功,见图3C~D。![]() 图 3 CRISPR/Cas9慢病毒感染MDA-MB-231和MDA-MB-468细胞的效率Figure 3 The efficiency of CRISPR/Cas9 lentivirus infection in MDA-MB-231 and MDA-MB-468 cells*: P<0.05, ****: P<0.0001. A: Fluorescence images of lentivirus-infected MDA-MB-231 cells (100×). The left side shows the images observed under visible light, and the right reveals those under fluorescence; B: The protein expression of CIB1 in CIB1-KD group was detected by Western blot; C: Fluorescence images of lentivirus-infected MDA-MB-468 cells (100×). The left side shows the images observed under visible light, and the right reveals those under fluorescence; D: The protein expression of CIB1 in CIB1-KD group was detected by Western blot.
图 3 CRISPR/Cas9慢病毒感染MDA-MB-231和MDA-MB-468细胞的效率Figure 3 The efficiency of CRISPR/Cas9 lentivirus infection in MDA-MB-231 and MDA-MB-468 cells*: P<0.05, ****: P<0.0001. A: Fluorescence images of lentivirus-infected MDA-MB-231 cells (100×). The left side shows the images observed under visible light, and the right reveals those under fluorescence; B: The protein expression of CIB1 in CIB1-KD group was detected by Western blot; C: Fluorescence images of lentivirus-infected MDA-MB-468 cells (100×). The left side shows the images observed under visible light, and the right reveals those under fluorescence; D: The protein expression of CIB1 in CIB1-KD group was detected by Western blot.2.3 敲低CIB1对乳腺癌细胞增殖的影响
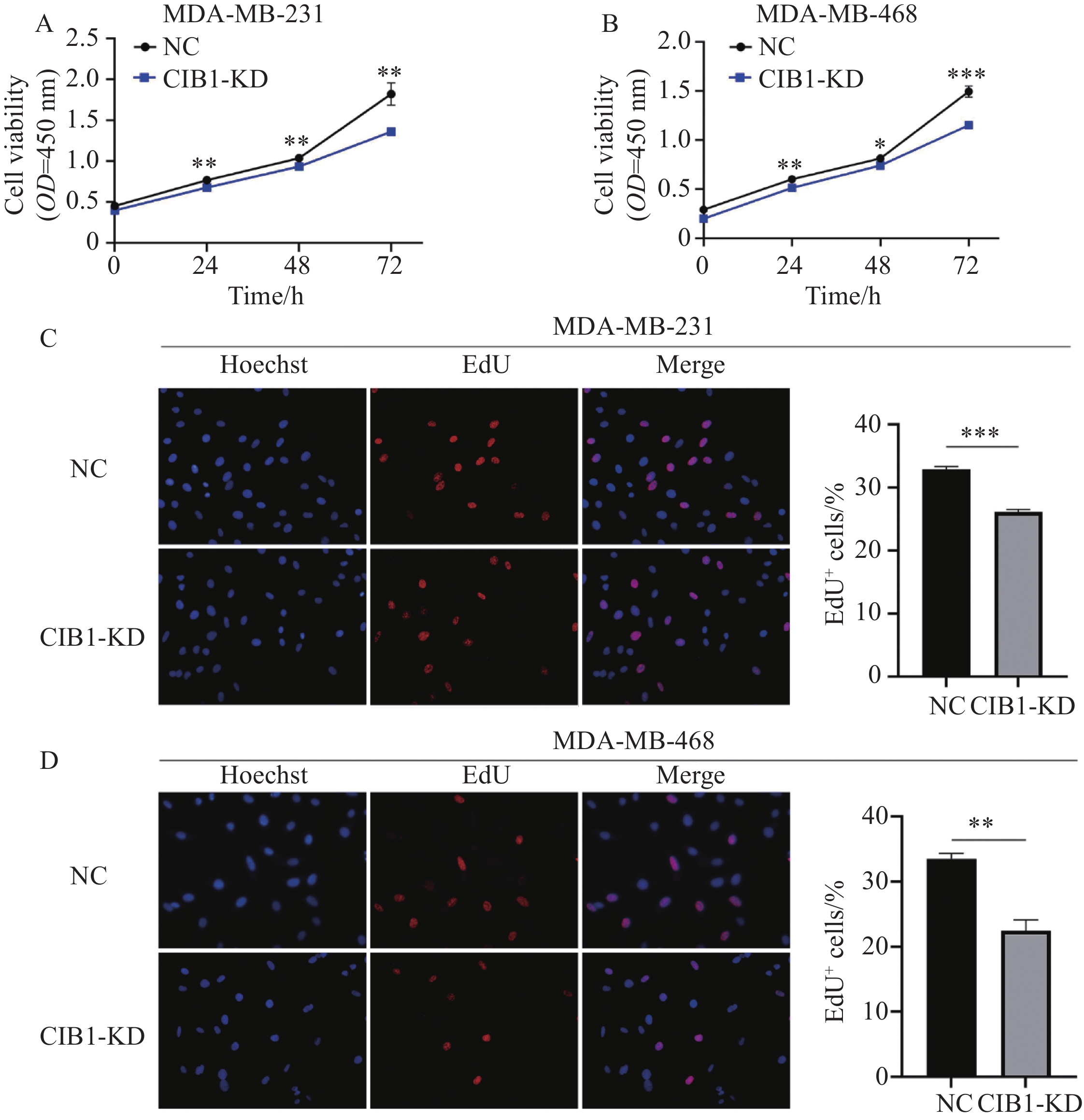
CCK-8实验结果显示,与NC组比较,MDA-MB-231和MDA-MB-468细胞中,感染24、48、72 h后,CIB1-KD组细胞增殖活性降低,24、48、72 h各时间点间差异具有统计学意义(P<0.05),见图4A~B。EdU实验检测结果显示,相较于NC组,两种细胞中CIB1-KD组EdU阳性率显著下降,t值分别为11.19和5.87,P值分别为
0.0004 和0.0042 ,差异均具有统计学意义(均P<0.01),见图4C~D。提示敲低CIB1可抑制MDA-MB-231和MDA-MB-468细胞增殖。2.4 敲低CIB1对MDA-MB-231和MDA-MB-468细胞凋亡的影响
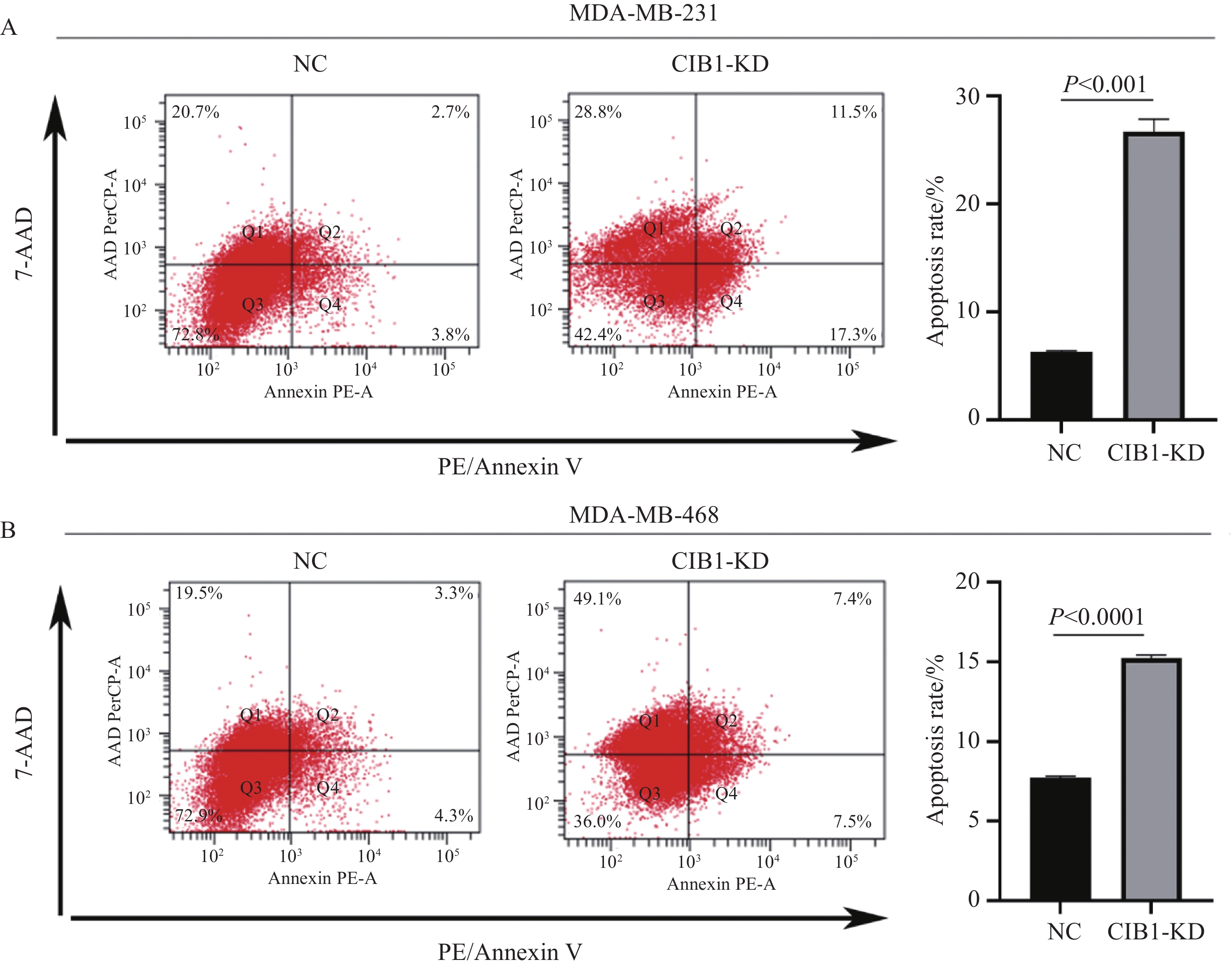
流式细胞仪检测结果表明,MDA-MB-231细胞CIB1-KD组的总体凋亡率高于NC组(26.70% vs 6.30%,t=13.32,P<0.001),而在MDA-MB-468细胞中,CIB1敲低组细胞凋亡率高于NC组(15.23% vs. 7.73%,t=33.92,P<
0.0001 ),差异均具有统计学意义,见图5。2.5 敲低CIB1对乳腺癌细胞迁移能力的影响
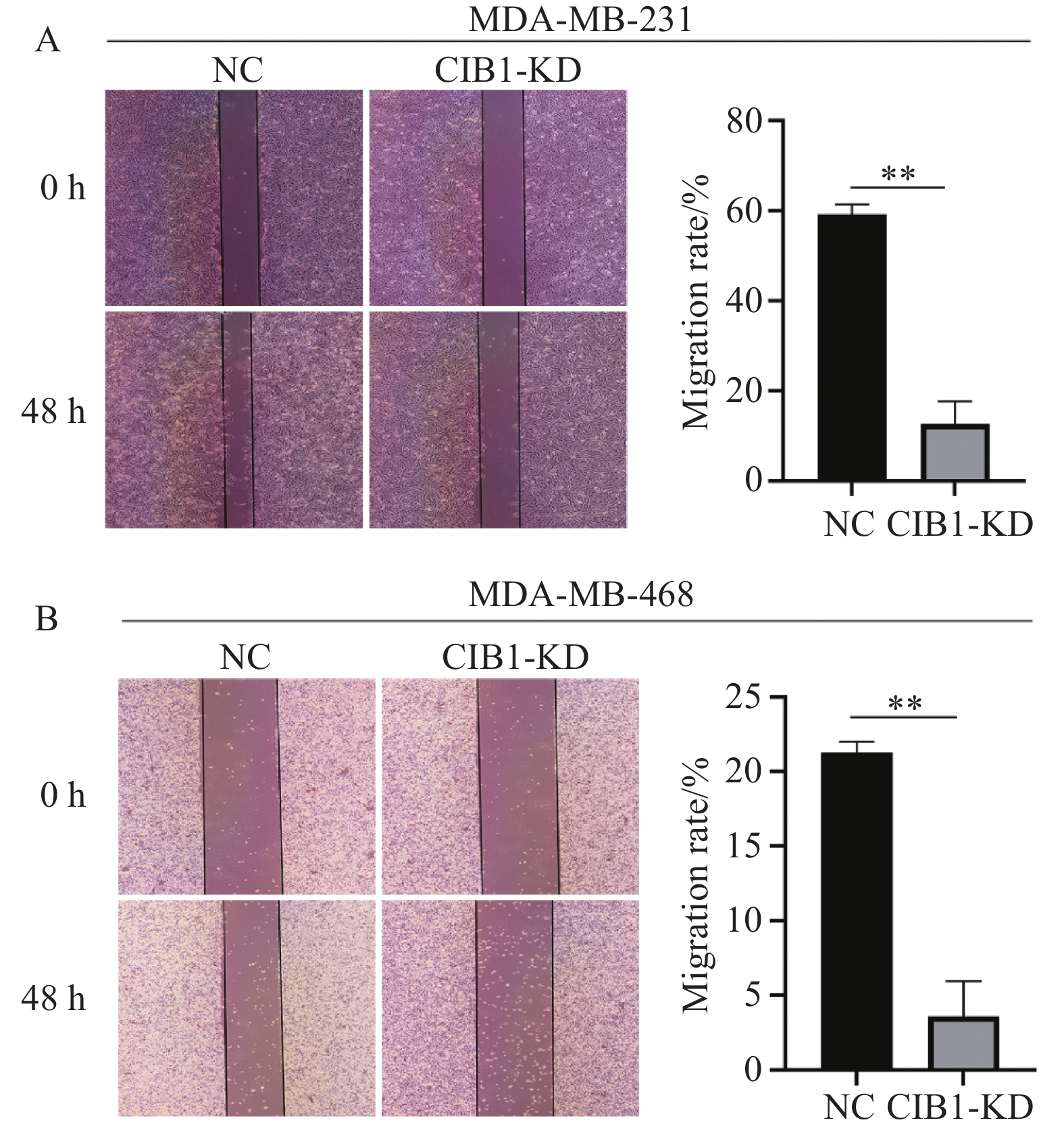
划痕实验结果提示,在MDA-MB-231和MDA-MB-468两种细胞中,CIB1-KD组迁移能力较NC组减弱,t=8.395、t=7.117,P=
0.0011 、P=0.0021 ,差异具有统计学意义,见图6。2.6 敲低CIB1对乳腺癌细胞侵袭能力的影响
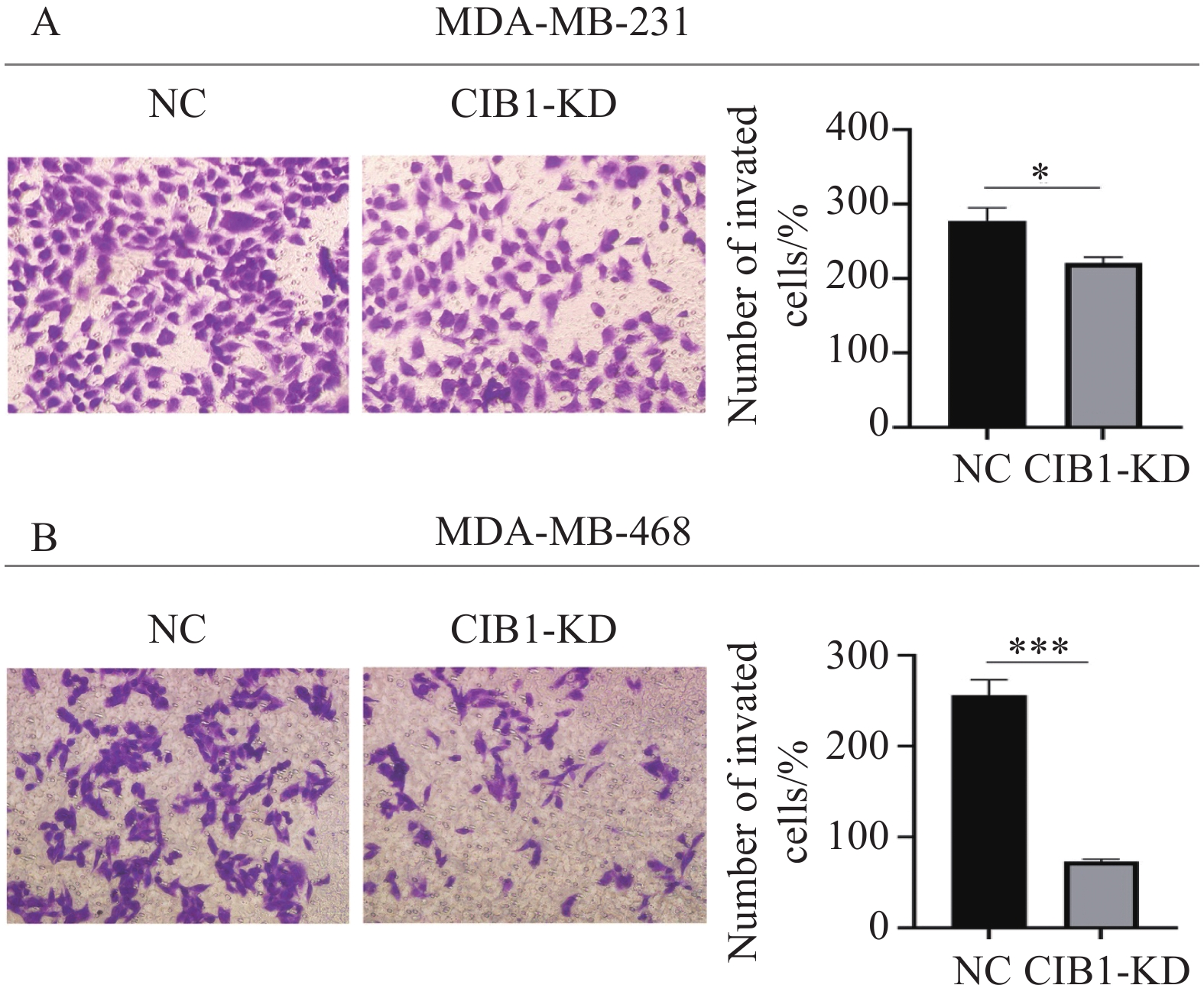
根据Transwell实验结果,在MDA-MB-231细胞中,同NC组比,CIB1-KD组细胞侵袭能力减弱(277.67 vs. 220.67,t=2.957,P=
0.0417 ),敲减CIB1的MDA-MB-468细胞侵袭能力比NC组显著减弱(73.00 vs. 256.00,t=10.38,P=0.0005 ),差异具有统计学意义(P<0.01),见图7。2.7 Wnt/β-Catenin信号通路关键因子的mRNA表达情况
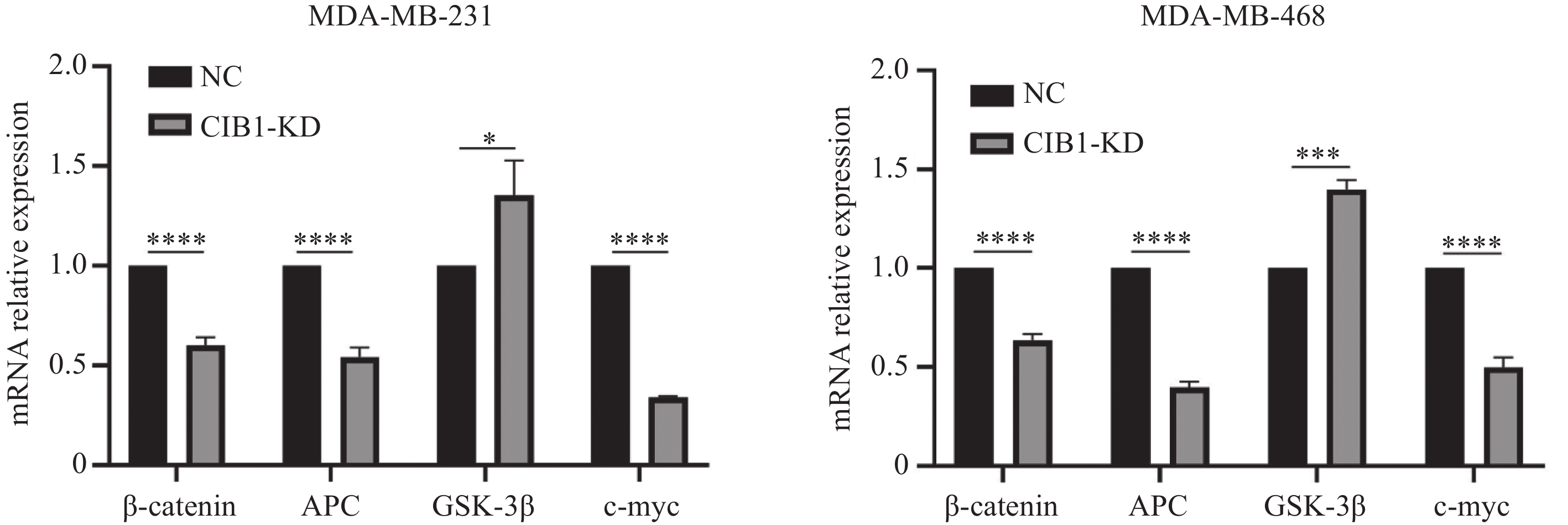
通过qRT-PCR实验检测Wnt/β-Catenin信号通路关键因子的mRNA相对表达,结果显示,同NC组对比,当CIB1表达量降低时,β-Catenin、APC、c-myc的mRNA相对表达降低(P<
0.0001 ),GSK-3β的mRNA相对表达增高(P<0.05),见图8。2.8 Wnt/β-Catenin信号通路关键因子的蛋白表达情况
Western blot实验结果显示,CIB1-KD组中β-Catenin、APC、p-GSK-3β(Ser9)、c-myc的蛋白相对表达量低于NC组(P<0.05),GSK-3β的蛋白相对表达高于NC组(P<0.05),见图9。
3 讨论
癌症基因组图谱(The Cancer Genome Atlas)项目让我们对乳腺癌靶向治疗有了新的认识[6],寻找分子治疗靶点和新的生物标志物对乳腺癌的早期诊断和基因靶向治疗具有重要意义。
钙和整合素结合蛋白1(CIB1),也被称为calmyrin和KIP,最初被鉴定为血小板整合素细胞质结构域α - IIb/β3(αIIbβ3)的结合伙伴,后来被发现能调节αIIbβ3的激活并下调肌醇1,4,5 -三磷酸受体依赖性钙离子的释放[7]。CIB1作为一种新兴的潜在癌基因,在多种人类癌症中广泛过表达[8]。CIB1可能通过调节Ca2+信号转导、端粒酶活性和DNA损伤,调节肿瘤细胞周期进程和促进肿瘤细胞增殖,抑制肿瘤细胞凋亡,介导肿瘤细胞迁移和血管生成等多种进程[9]。有研究发现,CIB1能促进TNBC细胞增殖[10],但CIB1在乳腺癌中的作用尚不完全明确。本研究通过对敲低CIB1的乳腺癌细胞系MDA-MB-231和MDA-MB-468细胞生物学行为进行检测,结果显示当CIB1被敲低时,MDA-MB-231和MDA-MB-468细胞增殖、侵袭和迁移能力降低,凋亡细胞增多。由此,我们推测CIB1在乳腺癌的发生和发展中发挥促癌作用,但其作用机制尚不明确。
Wnt/β-catenin信号通路在细胞增殖和分化等过程中发挥着重要作用,对癌症的发展具有重要意义。Wnt/β-catenin信号通路的异常激活已在多种癌症中被发现,如结直肠癌、胃癌和前列腺癌[11-13]。研究表明Wnt/β-catenin通路激活参与乳腺癌癌变[14]。转录因子β-连环蛋白(β-catenin)是Wnt/β-catenin信号通路的关键调控因子,β-catenin的异常调控可导致早期癌症的发生[15]。β-catenin在细胞质中的蛋白表达水平主要受两个因素的调控:一方面是β-catenin可在细胞膜上与E-cadherin和α-catenin形成蛋白复合物,形成细胞间的粘附连接[16];另一方面细胞质中的β-catenin水平主要受Axin/APC/GSK3β/CK1α降解复合物的调控,降解复合物的作用主要依赖于GSK3β的激酶活性。当GSK3β在Ser9位点被磷酸化时,GSK3β激酶的活性被抑制,导致β-catenin在细胞质中积累[17]。此外,Wnt信号介导的β-catenin增加可以在细胞增殖过程中启动许多癌基因蛋白的转录激活,如APC和c-myc[18]。然而,CIB1是否通过调控Wnt/β-catenin信号通路促进乳腺癌细胞增殖、迁徙和侵袭的相关机制尚不清楚。因此,我们通过对CIB1在乳腺癌中Wnt/β-catenin信号通路的作用研究发现,沉默CIB1可以抑制β-catenin、APC、c-myc的mRNA和蛋白表达水平,抑制p-GSK-3β(Ser9)的蛋白表达,促进GSK-3β的mRNA和蛋白的表达,由此表明,CIB1在乳腺癌中通过抑制Wnt/β-catenin途径的激活,降低下游基因表达,最终降低细胞增殖、侵袭和迁移的能力。
综上所述,本研究表明敲低CIB1能够抑制乳腺癌MDA-MB-231和MDA-MB-468细胞增殖、迁移和侵袭,促进细胞凋亡,其作用机制可能与抑制Wnt/β-Catenin信号通路的激活有关,其深入机制还需要进一步研究。
Competing interests: The authors declare that they have no competing interests.利益冲突声明:所有作者均声明不存在利益冲突。作者贡献:贾庆华:实验设计,论文撰写王晓宇:实验实施,文献查阅,论文校正张富婷:指导并协助完成细胞生物学实验,论文校正马 俊:指导并协助完成分子生物学实验牛廷献:基金支持,项目管理和指导,论文校正 -
表 1 引物序列
Table 1 Primer sequences
Gene name Sequence(5′→3′) β-catenin CCAGGTGGTGGTTAATAAGGCT CTCACGATGATGGGAAAGGTTA APC AGGCTGACAAGTCATCTGGGAAC CAGGCTGTGAGTGAATGATGTTG GSK-3β GTTAGCAGAGACAAGGACGGCA GCAATACTTTCTTGATGGCGAC c-myc GGTCTTCCCCTACCCTCTCAAC GCTGTGAGGAGGTTTGCTGTG GAPDH GGAAGCTTGTCATCAATGGAAATC TGATGACCCTTTTGGCTCCC -
[1] Bray F, Laversanne M, Sung H, et al. Global cancer statistics 2022: GLOBOCAN estimates of incidence and mortality worldwide for 36 cancers in 185 countries[J]. CA Cancer J Clin, 2024, 74(3): 229-263.
[2] Haberman VA, Fleming SR, Leisner TM, et al. Discovery and Development of Cyclic Peptide Inhibitors of CIB1[J]. ACS Med Chem Lett, 2021, 12(11): 1832-1839. doi: 10.1021/acsmedchemlett.1c00438
[3] Wang X, Yang Y, Cai WQ, et al. The Relationship of Sphingosine Kinase 1 With Pyroptosis Provides a New Strategy for Tumor Therapy[J]. Front Immunol, 2020, 11: 574990. doi: 10.3389/fimmu.2020.574990
[4] Chung AH, Leisner TM, Dardis GJ, et al. CIB1 depletion with docetaxel or TRAIL enhances triple-negative breastcancer cell death[J]. Cancer Cell Int, 2019, 19: 26. doi: 10.1186/s12935-019-0740-2
[5] Liu L, Zhang ZF, Xia XL, et al. KIF18B promotes breastcancer cell proliferation, migration and invasion by targeting TRIP13 and activating the Wnt/β-catenin signaling pathway[J]. Oncol Lett, 2022, 23(4): 112. doi: 10.3892/ol.2022.13232
[6] Jacobs AT, Martinez Castaneda-Cruz D, Rose MM, et al. Targeted therapy for breast cancer: An overview of drug classes and outcomes[J]. Biochem Pharmacol, 2022, 204: 115209. doi: 10.1016/j.bcp.2022.115209
[7] Shahab M, Wadood A, Zheng GJ. Strategies for Targeting CIB1: A Challenging Drug Target[J]. Curr Pharm Des, 2022, 28(28): 2343-2348. doi: 10.2174/1381612828666220728101812
[8] Ma J, Song Y, Zhuang T, et al. Identification of calcium and integrin-binding protein 1 as a reprogrammed glucose metabolism mediator to restrict immune cell infiltration in the stromal compartment of pancreatic ductal adenocarcinoma[J]. Front Immunol, 2023, 14: 1158964. doi: 10.3389/fimmu.2023.1158964
[9] Wang X, Peng X, Zhang X, et al. The Emerging Roles of CIB1 in Cancer[J]. Cell Physiol Biochem, 2017, 43(4): 1413-1424.
[10] Shahab M, Liang C, Duan X, et al. In silico Mutagenesis and Modeling of Decoy Peptides Targeting CIB1 to Obscure its Role in Triple-negative Breast Cancer Progression[J]. Curr Pharm Des, 2023, 29(8): 630-638. doi: 10.2174/1381612829666230327162852
[11] Voutsadakis IA. Targeting super-enhancer activity for colorectal cancer therapy[J]. Am J Transl Res, 2024, 16(3): 700-719. doi: 10.62347/QKHB5897
[12] Long Y, Wu J, Shen Y, et al. CAPG is a novel biomarker for early gastric cancer and is involved in the Wnt/beta-catenin signaling pathway[J]. Cell Death Discov, 2024, 10(1): 15. doi: 10.1038/s41420-023-01767-6
[13] Liu YM, Wu AD, Chen Y, et al. Gastrodin inhibits prostate cancer proliferation by targeting canonical Wnt/beta-catenin signaling pathway[J]. Med Oncol, 2023, 41(1): 32. doi: 10.1007/s12032-023-02254-9
[14] Hashemi M, Hasani S, Hajimazdarany S, et al. Biological functions and molecular interactions of Wnt/β-catenin in breast cancer: Revisiting signaling networks[J]. Int J Biol Macromol, 2023, 232: 123377. doi: 10.1016/j.ijbiomac.2023.123377
[15] Yu F, Yu C, Li F, et al. Wnt/β-catenin signaling in cancers and targeted therapies[J]. Signal Transduct Target Ther, 2021, 6(1): 307. doi: 10.1038/s41392-021-00701-5
[16] Wang P, Tong K, Li Y, et al. The role and mechanism of HIF-1α-mediated glypican-3 secretion in hypoxia-induced tumor progression in hepatocellular carcinoma[J]. Cell Signal, 2024, 114: 111007. doi: 10.1016/j.cellsig.2023.111007
[17] Shi Q, Kang K, Chen YG. Liquid-liquid phase separation drives the β-catenin destruction complex formation[J]. Bioessays, 2021, 43(10): e2100138. doi: 10.1002/bies.202100138
[18] Jin W, Wang X. PLAGL2 Promotes the Proliferation and Migration of Diffuse Large B-cell Lymphoma Cells via Wnt/β-catenin Pathway[J]. Ann Clin Lab Sci, 2022, 52(3): 359-366.



 下载:
下载: