Causal Association Between Omega-3 Fatty Acids and Risk of Breast Cancer: A Mendelian Randomization Study
-
摘要:目的
利用孟德尔随机化方法分析Omega-3脂肪酸与乳腺癌发病风险的因果关联。
方法对Omega-3脂肪酸与乳腺癌全基因组关联研究(GWASs)数据进行分析,筛选出与Omega-3脂肪酸相关的遗传位点作为工具变量(IVs)。使用逆方差加权(IVW)、MR-Egger、加权中位数、简单模式和加权模式等孟德尔随机化分析方法对Omega-3脂肪酸和乳腺癌发病风险间的因果关系进行评估。
结果共筛选出47个与Omega-3脂肪酸强相关的SNPs作为工具变量,IVW等分析方法均显示Omega-3脂肪酸与乳腺癌的发病风险间不存在因果关联(P>0.05)。MR-Egger回归分析等方法均未检测到明显的基因水平多效性(P=0.319),表明分析结果具有较高的敏感性和稳健性。
结论Omega-3脂肪酸与乳腺癌发病风险之间无因果关联。
-
关键词:
- Omega-3脂肪酸 /
- 乳腺癌 /
- 孟德尔随机化 /
- 全基因组关联研究
Abstract:ObjectiveTo explore the causal relationship between Omega-3 fatty acids and the risk of breast cancer via Mendelian randomization analysis.
MethodsAnalysis was conducted on data from genome-wide association studies (GWASs) on Omega-3 fatty acids and breast cancer. The selected instrumental variables (IVs) comprised genetic loci associated with Omega-3 fatty acids. Various Mendelian randomization analysis methods, including inverse-variance weighted (IVW) method, MR–Egger regression analysis, weighted median, simple models, and weighted models, were used to evaluate the causal relationship between Omega-3 fatty acids and the risk of breast cancer.
ResultsA total of 47 single-nucleotide polymorphisms strongly associated with Omega-3 fatty acids were selected as IVs. The analysis methods, including IVW method, revealed no causal relationship between Omega-3 fatty acids and the risk of breast cancer (P>0.05). Analysis methods, such as MR-Egger regression analysis, did not detect significant gene-level pleiotropy (P=0.319), which indicates the high sensitivity and robustness of analysis results.
ConclusionThe findings of this study suggest the absence of a causal relationship between Omega-3 fatty acids and the risk of breast cancer.
-
0 引言
癌症是当前全球面临的重大公共卫生挑战之一。乳腺癌是女性最为常见的癌症之一,且发病率呈逐年上升趋势。资料显示,2023年美国新增乳腺癌患者占所有女性恶性肿瘤的31%[1]。尽管目前对乳腺癌有手术、放化疗、内分泌治疗等多种治疗手段,但部分患者的预后仍不乐观[2]。因此,预防乳腺癌的发生至关重要。
Omega-3脂肪酸在人体的生理及病理过程中扮演着重要角色。它有助于维持细胞膜的健康,促进人体神经系统的正常发育等,还具有抗炎、抗氧化、抗血小板聚集等生物学活性,对于心血管、炎性反应性和自身免疫性疾病等具有重要的保护作用[3]。目前Omega-3脂肪酸与乳腺癌的发病风险之间的关系仍存在争议。Omega-3脂肪酸降低乳腺癌风险的机制主要包括减少促炎类花生酸和增加炎性反应消退衍生物;破坏质膜的脂筏以减少致癌蛋白信号的转导;激活质膜G蛋白受体GRP120,阻断核因子-κB (nuclear factor-kappa B,NF-κB)向细胞核的转移,致细胞凋亡增加[4]。Yorko等研究表明,Omega-3脂肪酸能够通过影响细胞膜组成,以及增加细胞内氧化应激等机制降低乳腺癌的发生风险[5]。但同时,一些研究表明Omega-3脂肪酸对乳腺癌的发生风险几乎没有影响[6]。因此,有必要进一步研究Omega-3脂肪酸与乳腺癌发病风险间的相关性。
孟德尔随机化(Mendelian randomization,MR)将与暴露危险因素相关的单核苷酸多态性位点 (single nucleotide polymorphisms,SNP)作为工具变量(instrumental variables,IVs),评估暴露因素与临床相关结果之间的因果关系[7]。相较于传统的观察性研究,MR能够有效减少因混杂因素以及反向因果关系等导致的偏倚,提供更为可靠的研究结果,已成为当前流行病学研究中的重要工具[8]。本研究旨在通过对全基因组关联研究(genome-wide association study,GWAS)进行MR分析,以探究Omega-3脂肪酸与乳腺癌发病风险间的因果关系。
1 资料与方法
1.1 数据来源
本研究中的数据均来自公开发表的GWAS汇总数据集(https://gwas.mrcieu.ac.uk),不需要额外的伦理批准和知情同意。所有患者的遗传背景均来自欧洲血统,且不分男女。其中,关于Omega-3脂肪酸的GWAS遗传数据来自英国生物样本库[9],包括114 999例患者和12 321 875个SNP位点。而乳腺癌的遗传数据则来自尼泊尔实验室(Neale Lab),共包括337 159例患者,涵盖了10 894 596个SNP,见表1。
表 1 Omega-3脂肪酸和乳腺癌的遗传数据信息Table 1 Genetic data on Omega-3 fatty acids and breast cancerID Sample SNP Population Data source Gender Omega-3 fatty acids met-d-Omega-3 114 999 12 321 875 European The UK Biobank Male/Female Breast cancer Ukb-a-55 337 159 10 894 596 European Neale Lab Male/Female 1.2 研究方法
1.2.1 工具变量筛选
首先,以P<5.0×10−8为标准筛选与Omega-3脂肪酸显著相关的SNPs作为工具变量(IVs)。设置参数连锁不平衡系数r2=0.001和区域宽度=10 000 kb以去除各IVs间的连锁不平衡干扰[10]。进一步筛选SNPs进行异质性检测,最终得到与Omega-3脂肪酸显著相关的有效SNPs作为IVs。将两个数据库中提取的数据进行合并,确保暴露因素和结果的效应值与相同的效应等位基因相对应。同时,收集每个SNP的相关信息用于后续的MR分析,包括主等位基因、等位基因频率、β系数、P值和标准误差(SEs)等。
1.2.2 弱工具变量检测
以F统计量来评估工具变量间是否存在弱工具量偏倚,当选择的工具变量强度F>10,认为不存在弱工具变量,其公式为F=(N−k−1)/k×R2/(1−R2) ,其中N为暴露的样本数量,k为工具变量的个数,R2为暴露数据库中工具变量解释变异的比例。R2 =2×(1−EAF)×EAF×β2,其中 EAF为效应等位基因频率,β为等位基因效应值[11]。
1.2.3 孟德尔随机化(MR)分析
基于“TwoSampleMR”R语言包(4.3.1版本)进行MR分析。采用逆方差加权(IVW)、MR-Egger、加权中位数、简单模式和加权模式等五种MR分析方法来评估Omega-3脂肪酸与乳腺癌发病风险之间的关联。其中,IVW方法在保证所有遗传变异的SNPs都是有效工具变量的前提下,将每个工具变量方差的倒数作为权重进行拟合,以检测水平多效性[12]。MR-Egger方法引入了截距项,当截距接近于零时,可以认为遗传多效性的影响较小[13]。加权中位数则通过将不同工具变量的估计效应按照权重进行排序,然后选择中位数作为最终估计效应[14]。简单模式和加权模式能够估计不同工具变量的效应,并将这些效应进行汇总以得到最终的估计效应。通过使用这些不同的MR分析方法,能够全面评估Omega-3脂肪酸与乳腺癌发病风险之间的因果关系,并获得更可靠的研究结果。
1.2.4 敏感性分析
本研究主要采用MR-Egger回归分析、留一法(Leave-one out)以及Cochran Q检验对MR结果进行敏感性分析。其中,MR-Egger法用于评估SNPs作为IV的潜在多效性效应。当MR-Egger回归截距项不为零或者截距项P>0.05时,认为存在多效性[13]。留一法通过逐一排除各个SNP来判断MR结果的稳定性[15]。IVW法和MR-Egger法中的Cochran Q检验则用于评估IVs间是否存在异质性[16]。
2 结果
2.1 工具变量
在去除连锁不平衡以及异质性的干扰后,我们最终获得了47个与Omega-3脂肪酸显著相关的有效 SNPs作为IVs。一般认为,当F>10时,说明因果关联受到弱工具变量偏倚影响的可能性比较小[17]。通过计算,我们得到的R2值为0.098,而对应的F统计量值为266.096,进一步支持了该47个SNPs作为有效IVs的可靠性。
2.2 孟德尔随机化分析
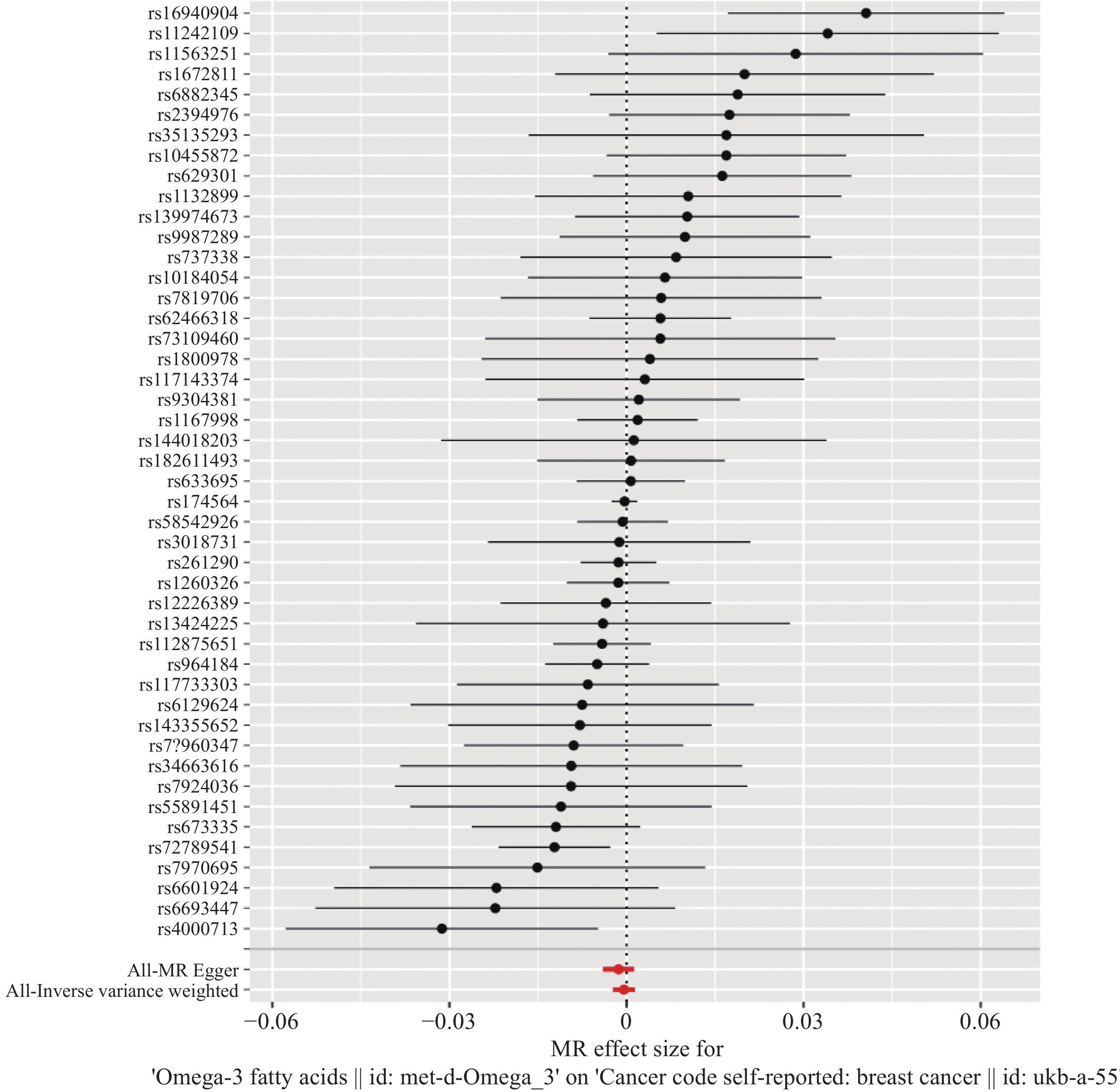
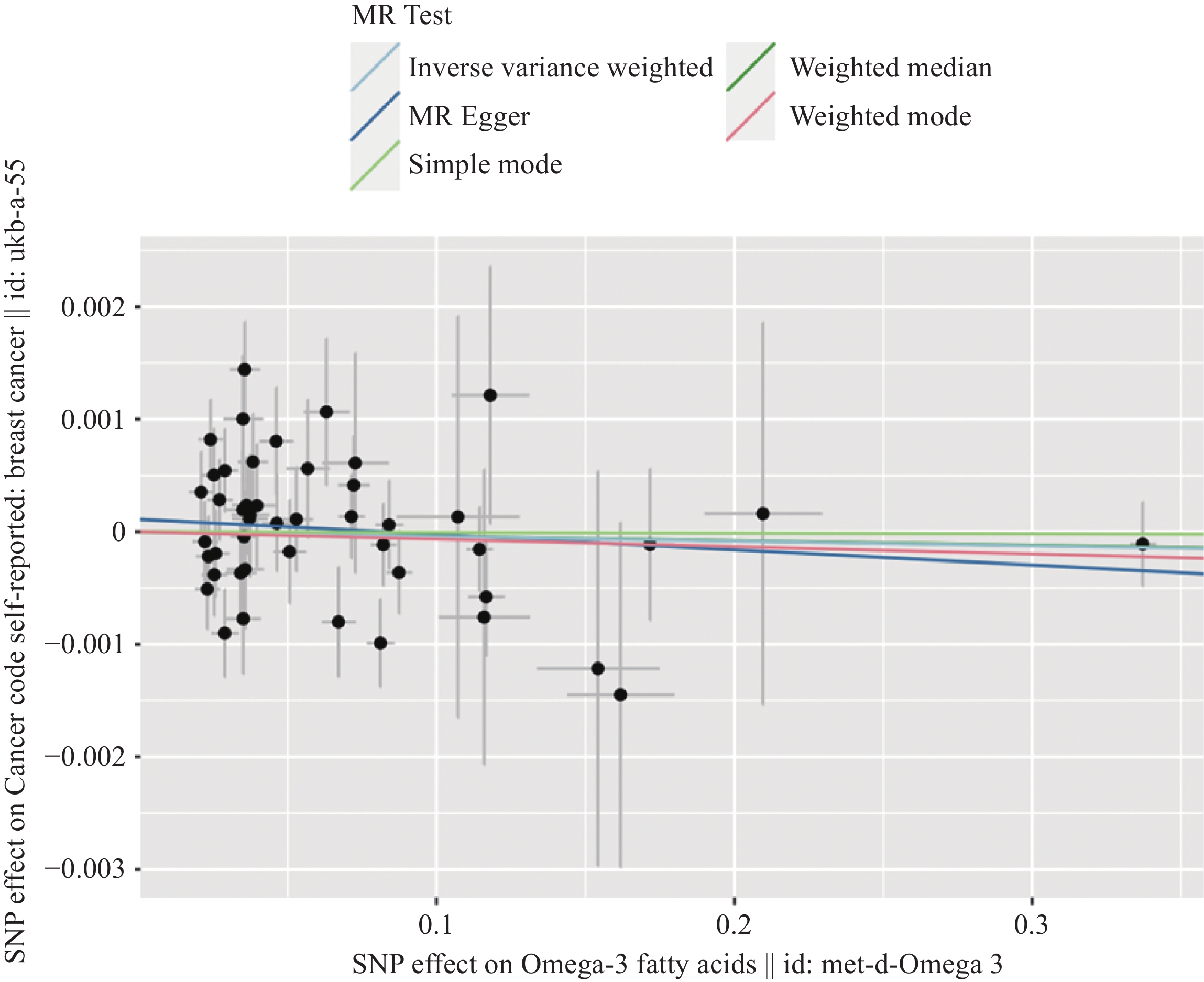
IVW、MR-Egger、加权中位数、简单模式及加权模式计算的Omega-3脂肪酸与乳腺癌发病风险之间的OR值以及95%CI值,见表2。根据分析结果,Omega-3脂肪酸与乳腺癌的发病风险间没有因果关系(均P>0.05),见表2、图1。五种方法得到的因果效应方向见图2。
表 2 Omega-3脂肪酸与乳腺癌发病风险因果关系孟德尔随机化IVW、MR-Egger回归、加权中位数、简单模式、加权模式分析Table 2 Association between Omega-3 fatty acids and risk of breast cancer analyzed using Mendelian randomization via IVW, MR-Egger regression, weighted median, simple model, and weighted modelMethods OR 95%CI P IVW 0.9996 0.998-1.001 0.66 MR-Egger regression 0.9986 0.996-1.001 0.31 Weighted median 0.9996 0.998-1.002 0.70 Simple mode 0.9999 0.995-1.005 0.98 Weighting model 0.9993 0.996-1.001 0.47 Notes: IVW: inverse variance weighting method; OR: dominance ratio; CI: confidence interval. 2.3 敏感性分析
2.3.1 异质性检验
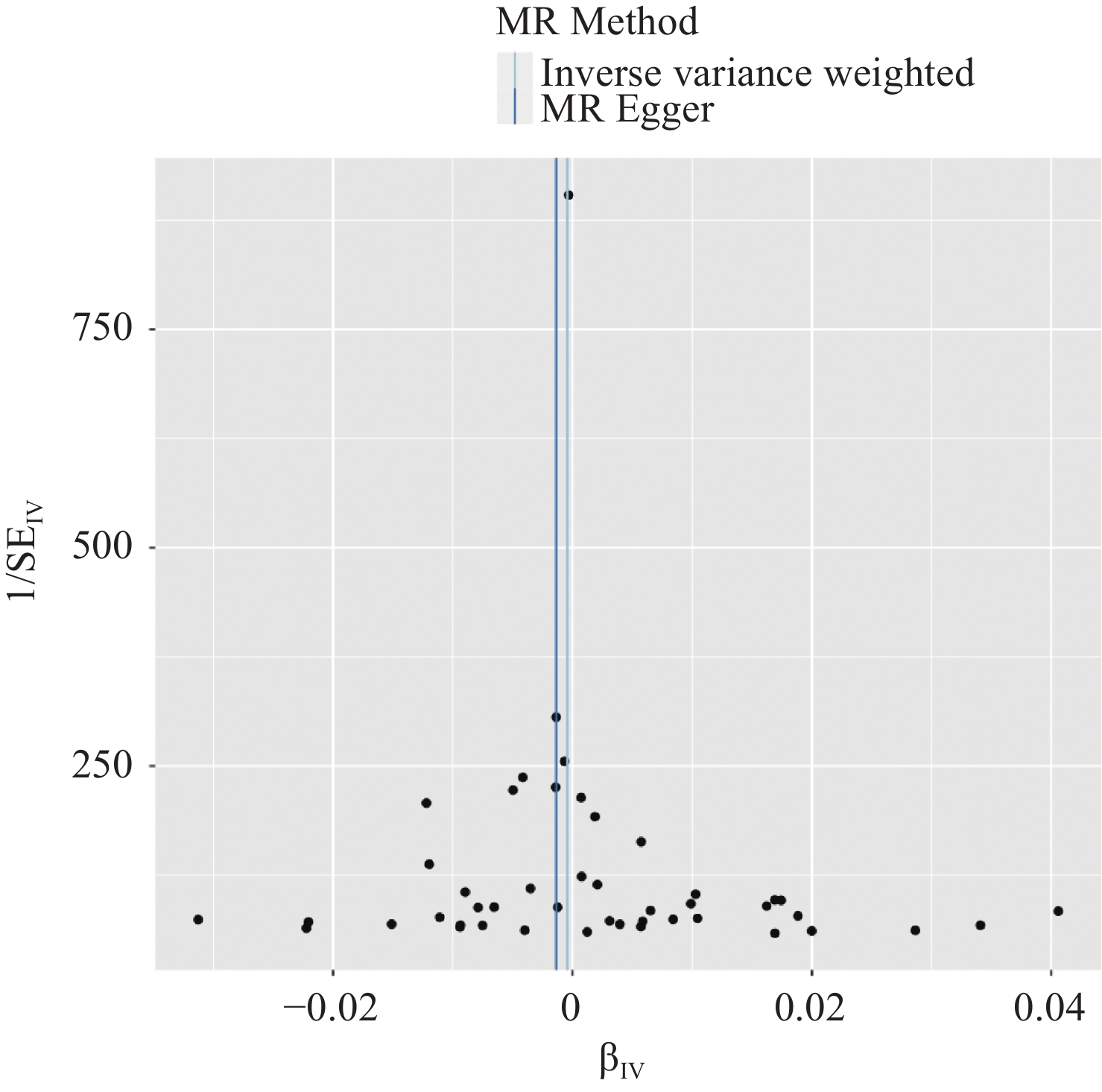
漏斗图结果显示,纳入的所有SNP基本对称,表明样本选择以及数据收集具有较好的代表性,见图3。然而,Cochran Q异质性检验在IVW(P=0.047)和MR-Egger回归(P=0.047)中的P值均小于0.05,表明纳入的SNPs可能存在异质性。异质性的存在并不违背MR的核心假设,但仍需进一步使用随机效应IVW模型方法进行计算,以确定其结果是否与IVW一致[18]。因此,本研究主要采用随机效应IVW模型计算结果。
2.3.2 多效性检验
MR-Egger回归分析得出P=0.319,截距项为
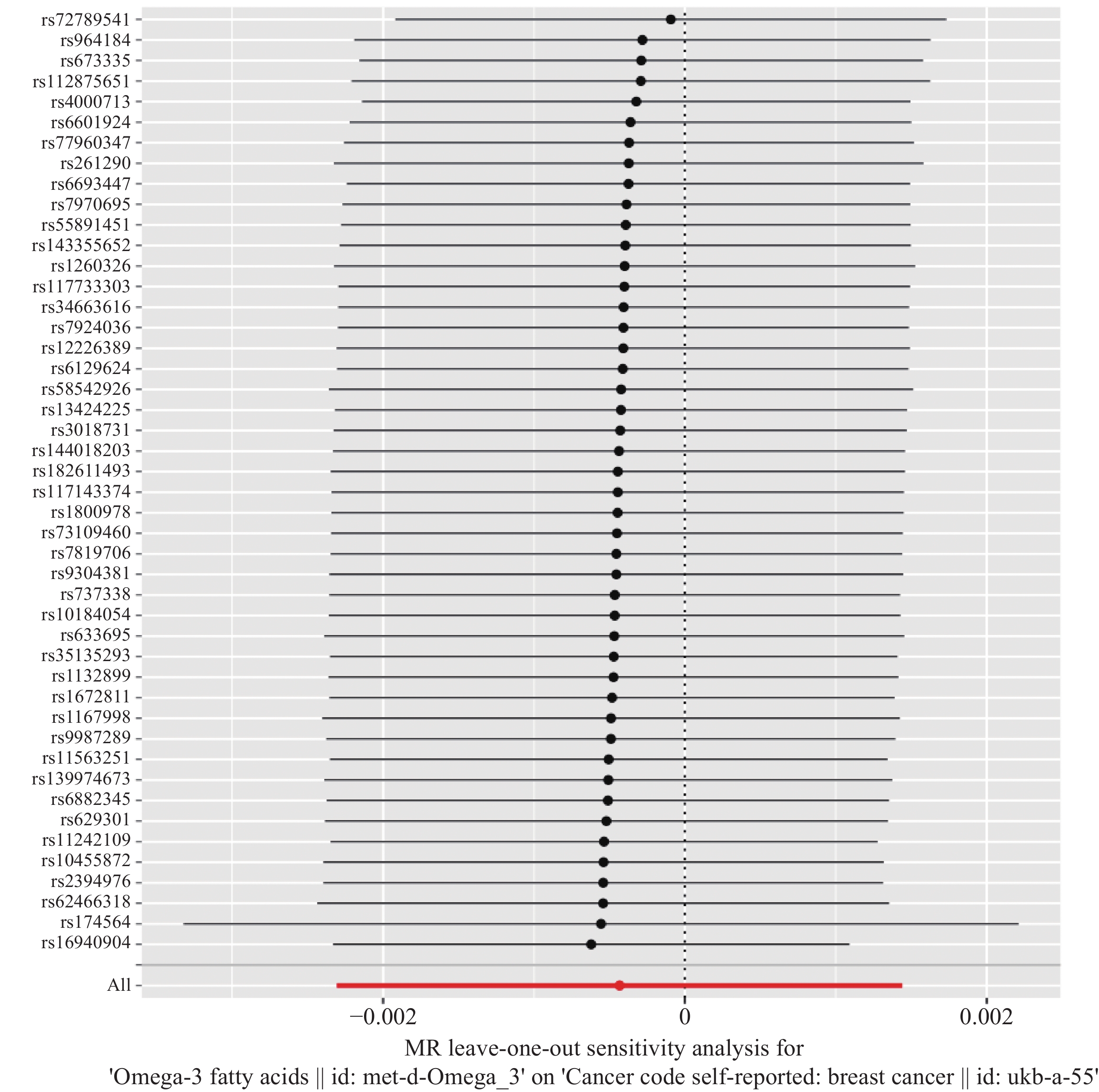
0.00011 ,接近于0,且P>0.05,表明MR分析结果受基因多效性的影响较小。2.3.3 “留一法”敏感性分析
逐个剔除每个SNP并重新计算,发现剩余SNPs的MR结果与总体结果之间没有显著差异。表明研究结果相对稳健,不受个别SNP的影响,见图4。
3 讨论
目前关于Omega-3脂肪酸对乳腺癌发病风险的影响仍存在争议。一些体外实验结果表明,Omega-3脂肪酸中的活性成分可能通过多种机制,如抑制炎性反应、干扰细胞信号通路、调节基因表达等,来抑制乳腺癌细胞的生长、凋亡以及转移[19-21]。此外,多项流行病学相关研究表明,高摄入Omega-3脂肪酸的人群乳腺癌的患病风险可能较低[22]。例如,在一项针对21项独立前瞻性队列研究的荟萃分析中,Zheng 等发现长期食用富含Omega-3脂肪酸的鱼油能够显著降低乳腺癌的发病风险。剂量反应分析表明,每天摄入Omega-3脂肪酸增加0.1克,患乳腺癌的风险降低5%[23]。然而,另外一些研究并未发现Omega-3脂肪酸与乳腺癌发病风险之间存在明显的相互关联[6,24]。本研究采用多种MR分析结果均表明,Omega-3脂肪酸对乳腺癌发病风险并无显著影响。此外,异质性检验、多效性检验等结果表明,我们的MR分析结果具有较高的稳健性。
本研究未发现Omega-3脂肪酸与乳腺癌的发病风险之间具有显著关系。但另有研究纳入Omega-3脂肪酸和Omega-6脂肪酸比值来分析对乳腺癌发病风险的影响。体内Omega-3脂肪酸和Omega-6脂肪酸可通过同时竞争相同的代谢途径(COX和LOX途径)来改变组织类花生酸的平衡、核因子κB介导的转录(NF-κB)和哺乳动物雷帕霉素靶标(mTOR)介导的信号转导等,从而影响乳腺肿瘤细胞的生长[25-27]。Yang等在一篇Meta分析中分析饮食摄入量时发现,膳食中每增加1/10的Omega-3/Omega-6脂肪酸比例,乳腺癌发病风险降低6%[28]。
本研究具备以下几点优势:(1)MR研究不易受传统观察类研究中常见的偏倚影响,如暴露测量误差、混杂因素和反向因果关系等[29]。(2)MR分析随机将参与者分为暴露组和非暴露组,类似于随机分配实验组和对照组。这有助于减少因个体特征差异而引起的偏倚。(3)本研究利用大规模GWAS汇总数据集,其中包含大量样本,这使我们能够更准确地评估Omega-3脂肪酸与乳腺癌之间的因果关系。
本研究也存在一定的局限性。首先,研究中样本均来源于欧洲血统,可能会对分析结果造成影响。有研究分析,海洋Omega-3脂肪酸在亚洲国家的保护作用比美国或欧洲国家更明显[23],因此,未来应当对其他种族人群进一步验证。其次,Omega-3脂肪酸可能对不同亚型乳腺癌产生不同影响,本研究所选择的Neale Lab数据未对乳腺癌亚型进行分组,无法对每种亚型的乳腺癌进一步分析。另外本研究未对绝经前后乳腺癌患者进行研究,目前关于Omega-3脂肪酸对绝经前后乳腺癌发病率的影响存在矛盾,有研究表明海洋Omega-3脂肪酸对乳腺癌的保护作用在绝经前妇女中比在绝经后妇女中更明显[30-31]。但也有研究显示,Omega-3脂肪酸摄入量与绝经后乳腺癌发病率呈显著负相关,但在绝经前妇女中则不然[23]。
综上所述,本研究通过MR分析提供了遗传证据,表明Omega-3脂肪酸与乳腺癌风险之间不存在因果关系。然而,仍需更多的大样本、前瞻性研究对我们的研究结果来进一步证实。
Competing interests: The authors declare that they have no competing interests.利益冲突声明:所有作者均声明不存在利益冲突。作者贡献:王嘉琪:设计研究方案、收集与统计数据、撰写及修改论文唐 伟:指导研究方案设计及数据统计分析黄 晓:指导论文修改符德元:指导研究方案设计及修改论文 -
表 1 Omega-3脂肪酸和乳腺癌的遗传数据信息
Table 1 Genetic data on Omega-3 fatty acids and breast cancer
ID Sample SNP Population Data source Gender Omega-3 fatty acids met-d-Omega-3 114 999 12 321 875 European The UK Biobank Male/Female Breast cancer Ukb-a-55 337 159 10 894 596 European Neale Lab Male/Female 表 2 Omega-3脂肪酸与乳腺癌发病风险因果关系孟德尔随机化IVW、MR-Egger回归、加权中位数、简单模式、加权模式分析
Table 2 Association between Omega-3 fatty acids and risk of breast cancer analyzed using Mendelian randomization via IVW, MR-Egger regression, weighted median, simple model, and weighted model
Methods OR 95%CI P IVW 0.9996 0.998-1.001 0.66 MR-Egger regression 0.9986 0.996-1.001 0.31 Weighted median 0.9996 0.998-1.002 0.70 Simple mode 0.9999 0.995-1.005 0.98 Weighting model 0.9993 0.996-1.001 0.47 Notes: IVW: inverse variance weighting method; OR: dominance ratio; CI: confidence interval. -
[1] Siegel RL, Miller KD, Wagle NS, et al. Cancer statistics, 2023[J]. Ca Cancer J Clin, 2023, 73(1): 17-48. doi: 10.3322/caac.21763
[2] Xia C, Dong X, Li H, et al. Cancer statistics in China and United States, 2022: profiles, trends, and determinants[J]. Chin Med J (Engl), 2022, 135(5): 584-590. doi: 10.1097/CM9.0000000000002108
[3] Fu Y, Wang Y, Gao H, et al. Associations among dietary omega-3 polyunsaturated fatty acids, the gut microbiota, and intestinal immunity[J]. Mediators Inflamm, 2021, 2021: 8879227.
[4] Fabian CJ, Kimler BF, Hursting SD. Omega-3 fatty acids for breast cancer prevention and survivorship[J]. Breast Cancer Res, 2015, 17(1): 62. doi: 10.1186/s13058-015-0571-6
[5] Yurko-Mauro K, Van Elswyk M, Teo L. A scoping review of interactions between omega-3 long-chain polyunsaturated fatty acids and genetic variation in relation to cancer risk[J]. Nutrients, 2020, 12(6): 1647. doi: 10.3390/nu12061647
[6] Hanson S, Thorpe G, Winstanley L, et al. Omega-3, omega-6 and total dietary polyunsaturated fat on cancer incidence: systematic review and meta-analysis of randomised trials[J]. Br J Cancer, 2020, 122(8): 1260-1270. doi: 10.1038/s41416-020-0761-6
[7] Ference BA, Holmes MV, Smith GD. Using Mendelian Randomization to Improve the Design of Randomized Trials[J]. Cold Spring Harb Perspect Med, 2021, 11(7): a040980. doi: 10.1101/cshperspect.a040980
[8] 王世浩, 付赛, 赵宇, 等. 两样本孟德尔随机化研究肾功能对骨质疏松症的因果关系[J]. 现代预防医学, 2022, 49(9): 1537-1542,1589. [Wang SH, Fu S, Zhao Y, et al. Investigating causal relations between renal function and osteoporosis: two sample Mendelian randomization study[J]. Xian Dai Yu Fang Yi Xue, 2022, 49(9): 1537-1542,1589.] doi: 10.3969/j.issn.1003-8507.2022.9.xdyfyx202209001 Wang SH, Fu S, Zhao Y, et al. Investigating causal relations between renal function and osteoporosis: two sample Mendelian randomization study[J]. Xian Dai Yu Fang Yi Xue, 2022, 49(9): 1537-1542,1589. doi: 10.3969/j.issn.1003-8507.2022.9.xdyfyx202209001
[9] Rusk N. The UK Biobank[J]. Nat Methods, 2018, 15(12): 1001.
[10] Hemani G, Zheng J, Elsworth B, et al. The MR-Base platform supports systematic causal inference across the human phenome[J]. Elife, 2018, 7: e34408. doi: 10.7554/eLife.34408
[11] Burgess S , Thompson GS. Mendelian Randomization: Methods for Causal Inference Using Genetic Variants[M]. Boca Raton: CRC Press, 2021.
[12] Burgess S, Bowden J, Fall T, et al. Sensitivity analyses for robust causal inference from Mendelian randomization analyses with multiple genetic variants[J]. Epidemiology, 2017, 28(1): 30-42. doi: 10.1097/EDE.0000000000000559
[13] Slob EAW, Groenen PJF, Thurik AR, et al. A note on the use of Egger regression in Mendelian randomization studies[J]. Int J Epidemiol, 2017, 46(6): 2094-2097. doi: 10.1093/ije/dyx191
[14] Bowden J, Holmes MV. Meta-analysis and Mendelian randomization: A review[J]. Res Synth Methods, 2019, 10(4): 486-496. doi: 10.1002/jrsm.1346
[15] Zheng J, Baird D, Borges MC, et al. Recent developments in Mendelian randomization studies[J]. Curr Epidemiol Rep, 2017, 4(4): 330-345. doi: 10.1007/s40471-017-0128-6
[16] Bowden J, Del Greco MF, Minelli C, et al. A framework for the investigation of pleiotropy in two-sample summary data Mendelian randomization[J]. Stat Med, 2017, 36(11): 1783-1802. doi: 10.1002/sim.7221
[17] Burgess S, Thompson SG. Bias in causal estimates from Mendelian randomization studies with weak instruments[J]. Stat Med, 2011, 30(11): 1312-1323. doi: 10.1002/sim.4197
[18] Nazarzadeh M, Pinho-Gomes AC, Bidel Z, et al. Plasma lipids and risk of aortic valve stenosis: a Mendelian randomization study[J]. Eur Heart J, 2020, 41(40): 3913-3920. doi: 10.1093/eurheartj/ehaa070
[19] Theinel M H, Nucci M P, Alves A H, et al. The effects of omega-3 polyunsaturated fatty acids on breast cancer as a preventive measure or as an adjunct to conventional treatments[J]. Nutrients, 2023, 15(6): 1310. doi: 10.3390/nu15061310
[20] Calder PC. Marine omega-3 fatty acids and inflammatory processes: Effects, mechanisms and clinical relevance[J]. Biochim Biophys Acta, 2015, 1851(4): 469-484. doi: 10.1016/j.bbalip.2014.08.010
[21] Osouli-Tabrizi S, Mehdizadeh A, Naghdi M, et al. The effectiveness of omega-3 fatty acids on health outcomes in women with breast cancer: A systematic review[J]. Food Sci Nutr, 2023, 11(8): 4355-4371.
[22] Nindrea R D, Aryandono T, Lazuardi L, et al. Protective effect of omega-3 fatty acids in fish consumption against breast cancer in Asian patients: a meta-analysis[J]. Asian Pac J Cancer Prev, 2019, 20(2): 327-332. doi: 10.31557/APJCP.2019.20.2.327
[23] Zheng JS, Hu XJ, Zhao YM, et al. Intake of fish and marine n-3 polyunsaturated fatty acids and risk of breast cancer: meta-analysis of data from 21 independent prospective cohort studies[J]. BMJ, 2013, 346: f3706. doi: 10.1136/bmj.f3706
[24] Lee KH, Seong HJ, Kim G, et al. Consumption of fish and ω-3 fatty acids and cancer risk: an umbrella review of meta-analyses of observational studies[J]. Adv Nutr, 2020, 11(5): 1134-1149. doi: 10.1093/advances/nmaa055
[25] Markosyan N, Smyth EM, Patrignani P, et al. Editorial: Eicosanoids in Cancer[J]. Front Pharmacol, 2021, 12: 765214. doi: 10.3389/fphar.2021.765214
[26] Wen ZH, Su YC, Lai PL, et al. Critical role of arachidonic acid-activated mTOR signaling in breast carcinogenesis and angiogenesis[J]. Oncogene, 2013, 32(2): 160-170. doi: 10.1038/onc.2012.47
[27] Song XD, Wang YN, Zhang A, et al. Advances in research on the interaction between inflammation and cancer[J]. J Int Med Res, 2020, 48(4): 0300060519895347.
[28] Yang B, Ren XL, Fu YQ, et al. Ratio of n-3/n-6 PUFAs and risk of breast cancer: a meta-analysis of 274135 adult females from 11 independent prospective studies[J]. BMC Cancer, 2014, 14: 105. doi: 10.1186/1471-2407-14-105
[29] Ran S, Yao J, Liu B. The association between sarcopenia and cirrhosis: a Mendelian randomization analysis[J]. Hepatobiliary Surg Nutr, 2023, 12(2): 291-293. doi: 10.21037/hbsn-22-632
[30] Guo F, Wang M, Guo X, et al. The association between fatty acid intake and breast cancer based on the NHANES and Mendelian randomization study[J]. Cancer Epidemiol, 2021, 73: 101966. doi: 10.1016/j.canep.2021.101966
[31] Zhang Z L, Ho S C, Liu K Y, et al. Association of dietary intake of n-3 polyunsaturated fatty acids with breast cancer risk in pre-and postmenopausal Chinese women[J]. Menopause, 2022, 29(8): 932-943. doi: 10.1097/GME.0000000000001990



 下载:
下载: