文章信息
- 吕梦果,颜次慧,宋新苗,曹水. 2015
- LV Mengguo, YAN Cihui, SONG Xinmiao, CAO Shui. 2015
- 骨桥蛋白预测早期非小细胞肺癌患者预后的意义
- Osteopontin Predicts Prognosis of Early Stage Non-small Cell Lung Cancer Patients
- 肿瘤防治研究, 2015, 42(04): 340-344
- Cancer Research on Prevention and Treatment, 2015, 42(04): 340-344
- http://www.zlfzyj.com/CN/10.3971/j.issn.1000-8578.2015.04.005
-
文章历史
- 收稿日期:2014-09-05
- 修回日期:2014-11-25
2.300060 天津,天津医科大学肿瘤医院生物治疗科
2. Department of Biotherapy, Tianjin Medical University Cancer Institute and Hospital, Tianjin 300060, China
肺癌是全球高发病率的恶性肿瘤之一,非小细胞肺癌(non-small cell lung cancer,NSCLC)约占肺癌的80%~85%[1]。近年来,肿瘤早期诊断技术和综合性治疗策略都有了很大进步,但其预后仍不能令人满意,约40%的早期患者会在术后出现局部复发或远处转移[2, 3]。目前,对非小细胞肺癌患者预后因素的研究进展缓慢。传统的临床病理特征如性别、年龄、分化程度和临床分期(tumornode-metastasis,TNM)等有助于评估患者的预后[4, 5],但这些因素仍不能准确评估患者的预后,即使是TNM分期相同的患者,其预后也不尽一致,这说明肿瘤的生物学行为存在异质性和复杂性。有研究表明骨桥蛋白(osteopontin,OPN)是参与调节肿瘤转移过程中的重要分子之一,OPN通过与整合素受体和CD44结合激活细胞核内的一系列信号通路,促进肿瘤局部进展或远处转移[6, 7]。本研究通过免疫组织化学法检测OPN在不同临床分期NSCLC患者癌组织中的表达情况,评估OPN表达与患者临床病理相关因素及预后的关系,特别是与早期患者预后的关系。1 资料与方法1.1 临床资料
84例NSCLC患者选自2004年6月—2010年12月天津医科大学附属肿瘤医院住院患者,均行外科手术并经病理学确诊。其中男52例、女32例,年龄35~77岁,中位年龄62岁。病理类型依据WHO肺癌组织学分类,鳞癌43例、腺癌41例。临床分期按UICC( 2009)分期标准:Ⅰ期27例、Ⅱ期22例、Ⅲ~Ⅳ期35例。1.2 免疫组织化学法
按EliVisionTM plus/HRP检测试剂盒说明书进行染色。将10%福尔马林固定、石蜡包埋的癌组织制成4~5 μm切片,进行常规脱蜡、水化,接着浸到0.01 mol/L、pH=6.0的枸橼酸盐缓冲液里,利用高压在130℃的环境下,行150 s 抗原修复。鼠抗人OPN多克隆抗体(SC-73631,美国Santa Cruz公司),稀释浓度1∶100,4℃孵育过夜。二抗(EliVisionTM plus 试剂盒,福建迈新公司)孵育30 min,DAB显色时间为90 s,利用苏木精进行细胞核染色,染色时间5 min。以已知阳性组织(乳腺浸润性导管癌)切片作为阳性对照,以磷酸盐缓冲溶液(PBS)代替一抗作阴性对照。1.3 OPN蛋白表达的判定标准
OPN蛋白阳性表达为肿瘤细胞质内产生棕黄色颗粒,由两位病理医师在不了解临床资料的前提下,对每张切片的免疫组织化学结果进行判定:随机观察5个高倍视野,计数100个细胞,依据阳性细胞比率及着色深度综合评定。无色为0分,淡黄色为1分,棕黄色为2分,棕褐色为3分;阳性细胞评分标准: 显微镜下随机取5个视野,根据每个视野中癌细胞或肺泡上皮细胞的阳性细胞比例进行评分,<1%为0分,1%~10% 为1分,>10%~30% 为2分,>30%为3分;总分=着色深度评分×阳性细胞比率评分,≤2分记为“-”,≥3分为“+”[8]。1.4 随访情况
所有患者均有完整的随访资料,通过复查病历及门诊登记电话的方式进行随访,随访截止日期为2013年10月1日,其中57例患者已死亡,27例患者存活。患者生存时间从手术确诊日期开始至死亡日期或随访截止日期,无病生存时间则以影像学检查(双锁骨上淋巴结B型超声,胸、肝、肾上腺CT、脑MR/CT、骨扫描检查)发现患者复发、远处转移为终点,两者均以月为单位计算。1.5 统计学方法
应用SPSS20.0 统计软件对所有资料行统计学分析,计数资料以率(%)表示,OPN在非小细胞肺癌组织中的表达情况与不同临床病理因素的组间比较采用χ2检验。生存分析利用Kaplan-Meier 生存曲线,并行Log rank 检验,检验水准α=0.05,以P<0.05为差异有统计学意义。2 结果2.1 肺癌组织中OPN的表达
84例非小细胞肺癌患者癌组织中OPN阳性表达率为83.3%(70/84),其中肺鳞状细胞癌阳性率81.4%(35/43),肺腺癌阳性率85.4%(35/41),见图 1。
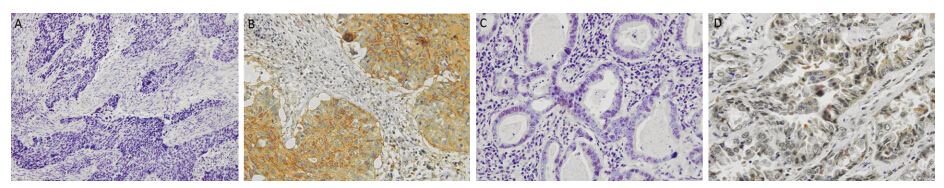 |
| A,C: negative expression of osteopontin(OPN) in squamous-cell carcinoma and adenocarcinoma; B,D: positive expression of OPN in squamous-cell carcinoma and adenocarcinoma 图 1 骨桥蛋白在非小细胞肺癌组织中的表达情况(SP×400)Figure 1 OPN expression in non-small cell lung cancer (NSCLC) tissues (SP×400) |
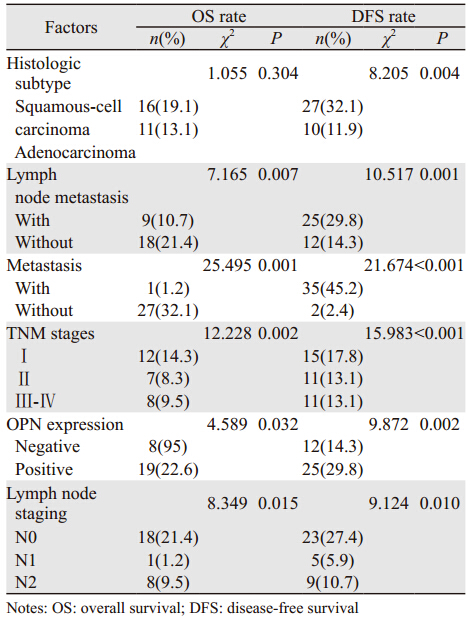
OPN表达与患者临床病理特征进行相关性分析结果。见表 1,OPN在Ⅰ期、Ⅱ期、Ⅲ~Ⅳ期患者阳性比例分别为77.8%、86.4%和85.7%。OPN表达与性别、年龄、有无吸烟、病理类型、有无淋巴结转移、有无远处转移、N分期和临床分期间比较差异无统计学意义,OPN表达与术后是否出现复发显著相关(χ2= 9.893,P=0.002)。
 |
84例NSCLC病例资料中,患者3年、5年总生存率分别为50.7%和31.5%,3年、5年无疾病生存率分别为41.7%和35.7%。Kaplan-Meier生存曲线显示: OPN阴性组的无疾病生存时间长于OPN阳性组(χ2=9.872,P=0.002),OPN阴性组的总生存时间长于阳性组(χ2=4.589,P=0.032),见图 2。单变量分析表明,有无淋巴结转移、有无远处转移、临床分期、N分期和OPN表达等因素是影响总生存率的不利因素;而OPN表达、病理类型、有无淋巴结转移和N分期、有无远处转移、临床分期等因素与无疾病生存率相关,见表 2。
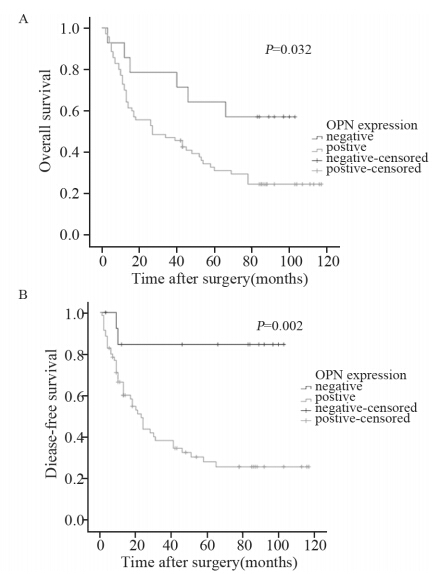 |
| A: Comparison of overall survival(OS) between OPN(-) group and OPN(+) group(P=0.032); B: Comparison of disease-free survival(DFS) between OPN(-) group and OPN(+) group (P=0.002)图 2 骨桥蛋白表达与患者预后关系的分析 Figure 2 Relationship between OPN expression and prognosis of NSCLC patients |
 |
为进一步探讨OPN表达在不同分期患者临床参数间有无差异,分析OPN表达与早期和晚期患者临床参数间关系。OPN表达与Ⅰ~Ⅱ期NSCLC患者术后是否出现复发显著相关(χ2=9.554,P= 0.002),与Ⅲ~Ⅳ期患者术后是否出现复发不相关。以3年为复发节点进一步分析,发现OPN表达与Ⅰ~Ⅱ期患者3年内是否复发相关(χ2= 6.271,P= 0.012)。
Ⅰ~Ⅱ期患者3年、5年总生存率分别为69.4%和48.9%,3年、5年无疾病生存率分别为63.3%和53.1%。通过Kaplan-Meier生存曲线分析:Ⅰ~Ⅱ期NSCLC患者,OPN阴性组的总生存时间和无疾病生存时间长于OPN阳性组(χ2=6.064,P= 0.014;χ2=9.722,P=0.019),见图 3。Ⅲ~Ⅳ期患者,OPN阴性组的总生存时间和无疾病生存时间与OPN阳性组间比较差异无统计学意义。
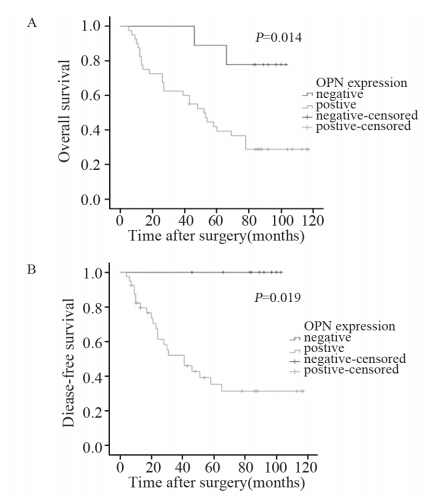 |
| A: Comparison of OS between OPN(-) group and OPN(+) group (P=0.014); B: Comparison of DFS between OPN(-) group and OPN(+) group(P=0.019) 图 3 骨桥蛋白表达与早期非小细胞肺癌患者预后的关系Figure 3 Relationship between OPN expression and prognosis of early stage NSCLC patients |
OPN是一种分泌型磷酸化糖蛋白,也被称作转化相关的磷酸酶蛋白,由Senger等[9]在上皮细胞株恶性转化中首次发现,OPN在细胞趋化、黏附和迁移、免疫调节、信号转导、抑制细胞凋亡等过程中均发挥重要作用[10]。近年来已有研究证实,在不同类型的恶性肿瘤中普遍存在OPN过表达的现象,而且血浆OPN水平与患者的不良预后密切相关,例如转移性乳腺癌患者的预后与血浆OPN水平和肿瘤负荷直接相关[11, 12],晚期肺癌患者血浆OPN水平与总生存时间和无进展时间呈负相关关系[13, 14]。但对OPN能否作为评估NSCLC预后的指标,特别是预测早期NSCLC患者预后的研究内容尚少。在此次研究中,我们证实NSCLC肿瘤组织中存在OPN高表达的现象,癌组织中OPN阳性表达率为83.3%,进一步分析发现OPN表达不仅与术后早期(3年内)复发显著相关,还与早期NSCLC患者的预后密切相关,OPN阳性表达的患者预后较差,复发风险高于OPN阴性表达的患者。
恶性肿瘤进展的关键是肿瘤细胞的复发转移,该过程涉及多种因素广泛参与调节,包括基因突变、活化下游信号通路、促进细胞外基质降解、肿瘤血管生成、肿瘤细胞增殖迁移等[15]。OPN是参与肿瘤发展的关键分子,其特征性结构是含有甘氨酸-精氨酸-甘氨酸-天冬氨酸-丝氨酸(Arg-Gly-Asp,RGD)的序列,通过与肿瘤细胞表面的整合素家族受体(αvβ3、αvβ5、αvβ1等)及CD44结合进而活化下游信号通路如磷脂酰肌醇3-激酶(PI-3'-kinase/AKT)、核因子κB(nuclear factor-κB,NF-κB)、基质金属蛋白酶(matrix metalloproteinases,MMPs)、尿激酶纤溶酶原激活物(uPA)等,介导肿瘤细胞间黏附、迁移和增殖;上调相关的效应因子如表皮生长因子(epidermal growth factor,EGF) 和血管内皮生长因子(vascular endothelial growth factor,VEGF),维持并促进肿瘤细胞增殖[16, 17]。
NSCLC是全球高发生率和高死亡率的恶性肿瘤之一,目前对其发生、发展机制的了解尚未十分透彻,对NSCLC预后判断的有效指标也不多,因此研究其发生和侵袭的分子机制在NSCLC早期诊断、有效治疗和改善预后等方面都具有积极意义。通过此次研究,我们发现OPN表达对预测早期NSCLC患者预后有重要意义,这也提示OPN可能是促进肿瘤进展、评估患者复发风险和预测患者预后的重要分子之一,OPN与其他能够评估患者预后的因素联合能为NSCLC患者早期疾病进展提供更多信息,更准确有效的评估患者预后[18, 19]。
综上所述,OPN蛋白在NSCLC的侵袭、转移及增殖过程中发挥重要作用,可能成为预测早期NSCLC患者预后的参考指标,为复发风险高的患者尽早提供个体化的治疗,干预肿瘤早期复发,延长患者生存时间。当然,此次研究收录的病例数有限,可能还需扩大不同分期的病例数,有待进一步研究验证。
| [1] | Siegel R, Ma J, Zou Z, et al. Cancer statistics, 2014 [J]. CA Cancer J Clin, 2014, 64(1): 9-29. |
| [2] | Chansky K, Sculier JP, Crowley JJ, et al. The International Association for the Study of Lung Cancer Staging Project: prognostic factors and pathologic TNM stage in surgically managed non-small cell lung cancer[J]. J Thorac Oncol, 2009, 4(7): 792-801. |
| [3] | Jin Y, Tong DY, Tang LY, et al. Expressions of Osteopontin (OPN), alphanubeta3 and Pim-1 Associated with Poor Prognosis in Nonsmall Cell Lung Cancer (NSCLC) [J]. Chin J Cancer Res, 2012, 24(2): 103-8. |
| [4] | Hoffman PC, Mauer AM , Vokes EE. Lung cancer [J]. Lancet, 2000, 355(9202): 479-85. |
| [5] | Gao W, Wang BC, Di JS, et al. COX regression analysis of the prognosis of Non-small Cell Lung Cancer [J]. Zhong Liu Yan Jiu Yu Lin Chuang, 2003, 15(2): 91-3. [高卫, 王宝成, 狄剑时, 等. 非小细胞肺癌预后因素的Cox回归分析[J]. 肿瘤研究与临床, 2003, 15(2): 91-3.] |
| [6] | Bogenrieder T, Herlyn M. Axis of evil: molecular mechanisms of cancer metastasis [J]. Oncogene, 2003, 22(42): 6524-36. |
| [7] | Wai PY, Kuo PC. Osteopontin: regulation in tumor metastasis[J]. Cancer Metastasis Rev, 2008, 27(1): 103-18. |
| [8] | Zhang J, Takahashi K, Takahashi F, et al. Differential osteopontin expression in lung cancer[J]. Cancer Lett, 2001, 171(2): 215-22. |
| [9] | Senger DR, Wirth DF, Hynes RO. Transformed mammalian cells secrete specific proteins and phosphoproteins[J]. Cell, 1979, 16(4): 885-93. |
| [10] | Rangaswami H, Bulbule A, Kundu GC. Osteopontin: role in signaling and cancer progression[J].Trends Cell Biol, 2006, 16(2): 79-87. |
| [11] | Rudland PS, Platt-Higgins A, El-Tanani M, et al. Prognostic significance of the metastasis-associated protein osteopontin in human breast cancer[J]. Cancer Res, 2002, 62(12): 3417-27. |
| [12] | Bramwell VH, Doig GS, Tuck AB, et al. Serial plasma osteopontin levels have prognostic value in metastatic breast cancer[J]. Clin Cancer Res, 2006, 12(11 Pt 1): 3337-43 |
| [13] | Hu Z, Lin D, Yuan J, et al. Overexpression of osteopontin is associated with more aggressive phenotypes in human non-small cell lung cancer[J]. Clin Cancer Res, 2005, 11(13): 4646-52. |
| [14] | Mack PC, Redman MW, Chansky K, et al. Lower osteopontin plasma levels are associated with superior outcomes in advanced non-small-cell lung cancer patients receiving platinum-based chemotherapy: SWOG Study S0003[J]. J Clin Oncol, 2008, 26(29): 4771-6. |
| [15] | Shevde LA, Das S, Clark DW, et al. Osteopontin: an effector and an effect of tumor metastasis[J].Curr Mol Med, 2010, 10(1): 71-81. |
| [16] | El-Tanani MK. Role of osteopontin in cellular signaling and metastatic phenotype[J]. Front. Biosci, 2008, 13: 4276-84. |
| [17] | Anborgh PH, Mutrie JC, Tuck AB, et al. Role of the metastasispromoting protein osteopontin in the tumour microenvironment [J]. J Cell Mol Med, 2010, 14(8): 2037-44. |
| [18] | Johnston NI, Gunasekharan VK, Ravindranath A, et al. Osteopontin as a target for cancer therapy[J]. Front Biosci, 2008, 13: 4361-72. |
| [19] | Weber GF. The cancer biomarker osteopontin: combination with other markers[J]. Cancer Genomics Proteomics, 2011, 8(6): 263-88. |
 2015, Vol. 42
2015, Vol. 42


