文章信息
- 吴昕,刘磊,段宝凤,张恒丽,杨莉,李平. 2014.
- WU Xin, LIU Lei, DUAN Baofeng, ZHANG Hengli, YANG Li, LI Ping. 2014.
- PGC方案诱导化疗后同步放化疗治疗Ⅲ~ⅣA期鼻咽癌的Ⅱ期单中心前瞻性临床研究
- A Prospectively Monocentric Phase Ⅱ Clinical Analysis on PGC Induction Chemotherapy Followed by Concurrent Chemoradiotherapy for Stage Ⅲ-ⅣA Nasopharyngeal Carcinoma Patients
- 肿瘤防治研究, 2014, 41(09): 998-1001
- Cancer Research on Prevention and Treatment, 2014, 41(6): (09): 998-1001
- http://www.zlfzyj.com/CN/10.3971/j.issn.1000-8578.2014.09.010
-
文章历史
- 收稿日期:2013-11-29
- 修回日期:2014-03-21
鼻咽癌(NPC)流行病学方面有特征性的地域 分布,如东南亚和地中海盆地高发,其年发病率高 达(20~30)/10万人[1]。鼻咽癌不同于其他头颈部 肿瘤,手术不作为首选根治方案。早期鼻咽癌患者 单纯放疗可以达到根治的疗效,但对于局部晚期 (T3,T4)及较大淋巴结转移患者,单纯放疗疗效 差,报道5年生存率在34%~52%之间[2]。因此,需 要联合化疗来提高局部、区域控制率及总生存率。 化疗分为新辅助化疗、同步化疗、辅助化疗。放疗 同步铂类化疗已成标准治疗模式。有报道诱导化疗 加同步放化疗可进一步提高局部晚期无进展鼻咽癌 展生存期、无复发生存期和总的生存期[3]。
与头颈部鳞癌相似,鼻咽癌的最常见化疗方案 为5-氟尿嘧啶联合顺铂,有效率为55%~65%。中位 疾病进展时间为6~8月[4]。近年来紫杉醇、吉西他 滨、卡铂等药物治疗鼻咽癌患者疗效逐渐得到肯 定。单药有效率分别为: 34%~45%、43%、44%[5, 6, 7]。 其中紫杉醇联合卡铂有效率为75%[8],吉西他滨联合 卡铂有效率为64%[9]。基于两药方案比单药化疗有 效率高及两药方案耐受较好,我们选取对鼻咽癌有 效并且作用机制不同的三种化疗药物联用,希望有 更高的有效率以及可耐受的不良反应。
本研究尝试采用脂质体紫杉醇、吉西他滨、卡铂 这种新颖的诱导化疗联合同步放化疗,治疗中晚期鼻 咽癌患者,取得较满意的效果,现将结果报告如下。 1 资料与方法 1.1 纳入标准
患者必须经鼻咽纤维镜取活检病理证实为鼻咽 低分化鳞癌。根据第七版AJCC标准分期[10]为Ⅲ~ⅣA 期,未接受过放化疗的初治患者。年龄在18~70岁, 体力状况评分(eastern cooperative oncology group, ECOG) ≤1分。白细胞>4×109/L,中性粒细胞>2×109/ L,血小板>8×109/L,血红蛋白>9 g/L。肝功谷草转氨 酶(ALT)及谷丙转氨酶(AST)<正常值的两倍。肾 功能:血清肌酐<140 mol/L。无严重感染,无其他系 统严重疾病,无妊娠。所有患者签署知情同意书。 1.2 患者基本特征
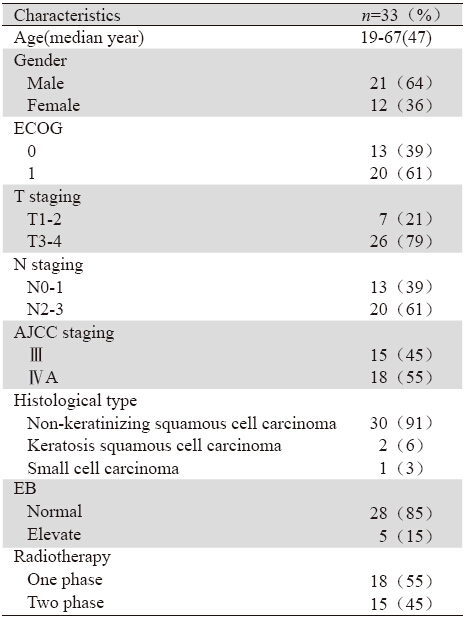
从2012年5月10月,共33例患者入组,其基本 特征见表 1。
患者治疗前需行详细病史采集和查体、血常 规及生化检查、EB病毒检测、12导联心电图检 查、增强鼻咽及颈部MRI和鼻咽纤维镜检查、胸 部平扫CT、上腹部彩超检查、骨扫描。 1.4 治疗方案 1.4.1 化疗
2周期PGC方案新辅助化疗。用药标 准脂质体紫杉醇(力朴素)135 mg/m2配5%的葡萄 糖溶液500 ml,3 h内静脉滴入;吉西他滨(泽菲) 1000 mg/m2配0.9%氯化钠溶液100 ml 30 min内静 脉滴入;卡铂,按血药浓度-时间曲线下面积(area under the curve,AUC)和肌酐清除率来计算卡铂 的剂量:根据Calvert公式进行。卡铂剂量(mg)= 所设定的AUC(mg/ml/min)×[肌酐清除率(ml/ min)+25]。AUC(mg/ml/min)取值5。配5%的葡 萄糖溶液500 ml;第一天给药,每周期21天。所有患者在脂质体紫杉醇前静推地塞米松10 mg,预防过敏反应,并给予昂丹司琼止吐,奥美拉唑抑制胃酸分泌等对症处理。2周期化疗完成后给予放疗,同步给予卡铂,AUC取5,化疗D1,D21,D42。
如果中性粒细胞<1.5×109/L,血小板<80×109/L, 给予粒细胞集落刺激因子、巨核细胞集落刺激因子 对症治疗。如果Ⅳ度中性粒细胞下降持续3天,或Ⅲ 度血小板下降持续3天,下一周期化疗减量20%。如 果ALT、 AST大于正常值的两倍,给予保肝治疗;如 果肌酐>140 mol/L,暂停化疗,2周后再行评价。 1.4.2 放疗
采用6 MV-X,调强放射治疗,每 日一次,每周5次。按照ICRU 62号报告[11]及中 国鼻咽癌共识来勾画靶区,放疗处方:GTVnx 74Gy/33F,2.24Gy/F; GTVnd 70Gy/33F,2.12Gy/ F; CTV1 60Gy/33F,1.8Gy/F; CTV2 56Gy/33F, 1.7Gy/F; CTVnd 56Gy/33F,1.7Gy/F[12] ,见表 2。
放化疗中每周门诊随访,复查血常规、生 化,查体,记录不良反应及分级,评价患者耐受 性。2周期化疗后复查MRI评价诱导化疗疗效; 放疗完成后复查增强鼻咽及颈部MRI、鼻咽纤维 镜;放疗完成3月及1年后再次复查增强鼻咽及颈 部MRI、鼻咽纤维镜、胸部平扫CT、上腹部彩超 检查和骨扫描,评价放化疗近期疗效和1年无病生存,总生存。肿瘤治疗效果按照实体瘤疗效评价 标准RECIST标准[13]进行评价,不良反应按照WHO 和RTOG不良反应分级标准进行评价。 2 结果 2.1 疗效
所有的患者均按照治疗计划进行治疗。在 PGC诱导化疗两周期后,进行复查评价。7例 (21%)患者完全缓解(CR),21例(64%) 患者部分缓解(PR),4例(12%)患者稳定 (SD),1例(3%)患者进展(多发性肺转移)。
放疗完成后,复查增强鼻咽及颈部MRI和鼻咽 纤维镜,24(例73%)患者完全缓解(CR),7例 (21%)患者部分缓解(PR),1例(3%)患者稳 定(SD),1例(3%)患者进展(多发性肺转移)。
放疗完成3月后,全面复查,确认疗效。28例 (85%)患者完全缓解(CR),4例(12%)患者部分缓 解(PR),1例(3%)患者进展(多发性肺转移)。放疗 完成1年后随访,30例(91%)患者完全缓解(CR),3 例(9%)患者进展(多发肺转移2例,多发腰椎转移1 例)。1年总生存率100%,1年无病生存率91%。 2.2 不良反应
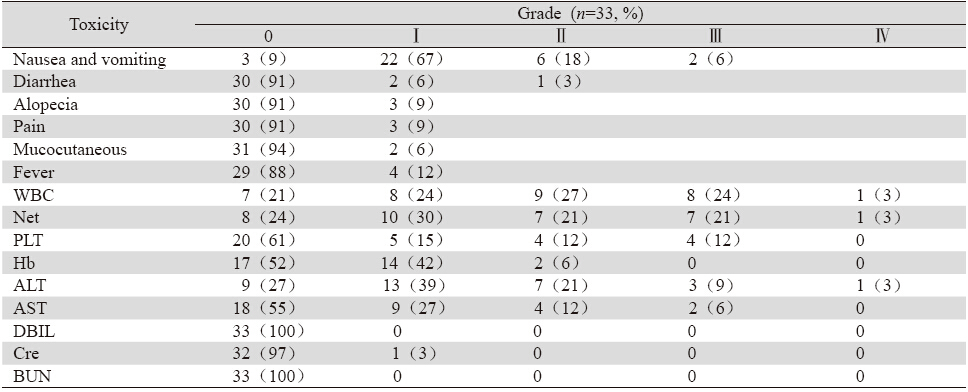
PGC新辅助化疗最常见的不良反应为骨髓抑 制及胃肠道反应。其中,9例(27%)患者发生Ⅲ ~Ⅳ级白细胞下降,粒细胞下降性发热1例。4例 (12%)发生Ⅲ度血小板减少反应。血红蛋白减 少均为Ⅰ~Ⅱ级。消化道反应中,恶心呕吐仅有2 例(6%)为Ⅲ级,腹泻仅有2例(6%)有轻微腹 泻。肝功能Ⅲ~Ⅳ级反应4例(12%),皮疹2例 (6%),疼痛发生率仅为3例(9%),见表 3。
 |
诱导化疗可以提高中晚期鼻咽癌的局部控制率 并延长生存时间。诱导化疗的优点包括:(1)肿瘤未 受放射治疗影响,血供良好,药物易于到达肿瘤部 位;(2)可降低肿瘤负荷,改善血供,提高放射敏感 度;(3)患者身体状况较好,易于耐受正规强烈化 疗;(4)有利于消灭亚临床病灶,提高生存率。
目前,诱导化疗没有标准的方案。单药化疗疗 效较差,双药化疗是主要的研究方向。研究报道三 药及三药以上化疗方案有效率较高[14, 15, 16]。TPF方案 应用较普遍,但是顺铂的消化道反应较大,5-Fu黏 膜反应较大,导致放疗中口腔黏膜反应较重,患者 耐受较差。因此,需要继续寻找其他有效低毒的三 药化疗方案。Leong等[17]进行三药化疗治疗复发鼻 咽癌,纳入28例复发转移的鼻咽癌患者,进行PGC方案化疗(吉西他滨 1 000 mg/m2+紫杉醇70 mg/m2+卡铂 AUC=2.5),D1/D8,21天重复,总有效率 为86%,CR率为11%。我们选用PGC(脂质体紫杉 醇、吉西他滨、卡铂)方案进行诱导化疗,是考虑 可以更好的利用三种抗肿瘤药物不同的作用机制, 提高疗效降低不良反应。紫杉醇属有丝分裂中的微 管抑制剂,可阻断细胞于细胞周期的G2与M期,使 癌细胞复制受阻断而死亡。但紫杉醇难溶于水,易 溶于聚氧乙基代蓖麻油(Cemophor EL)与无水乙 醇的混合溶酶中,其中Cemophor EL 能释放组胺, 导致过敏反应;还可在血液中形成微小颗粒包裹紫 杉醇分子,影响药物分子向组织间扩散,影响抗肿 瘤效应。脂质体紫杉醇是以脂质体双分子层包封紫 杉醇,避免溶酶导致的过敏反应,减少不良反应; 同时增加了水溶性,提高其在机体的靶向性[18, 19]。 盐酸吉西他滨属细胞周期特异性抗肿瘤药。主要杀 伤处于S期(DNA合成)的细胞,同时也阻断细胞 增殖由G1向S期过渡的进程。卡铂是周期非特异性 抗癌药,直接作用于DNA,主要与细胞DNA的链 间及链内交联,破坏DNA而抑制肿瘤的生长。卡 铂与顺铂相比,有更低的中性粒细胞及肾毒性,使 较大剂量的化疗可以耐受[5, 20]。本研究纳入局部晚 期鼻咽癌患者33例,均进行2周期PGC方案诱导化 疗。诱导化疗后CR 21%,PR 64%,(CR+PR)达 到85%。放疗完成3月后,确认疗效:CR 85%,PR 12%。结果优于双药方案诱导化疗。PGC新辅助化 疗最常见的不良反应为骨髓抑制及胃肠道反应。其 中,9例患者发生Ⅲ~Ⅳ级白细胞下降,粒细胞下降 性发热1例。4例发生Ⅲ度血小板减少反应。血红蛋 白减少不严重。血液血毒性易于控制,通过集落刺 激因子或适当调整化疗剂量,患者均能在1周内恢 复,未出现严重感染或死亡病例。使用粒细胞集落 刺激因子。消化道反应中,恶心呕吐反应经5-羟色 胺受体拮抗剂处理后均能耐受,腹泻不严重。肝功 能Ⅲ~Ⅳ级反应4例,经保肝药物治疗后好转。肾功 能损伤,脱发,过敏,疼痛较少。
综上,脂质体紫杉醇、吉西他滨、卡铂三药化疗 方案诱导化疗加同步放化疗治疗局部晚期鼻咽癌,有 效率较高、不良反应可以耐受,是一种可行的方案。
| [1] | Airoldi M, Gabriele AM, Garzaro M,et al. Induction chemotherapy with cisplatin and epirubicin followed by radiotherapy and concurrent cisplatin in locally advanced nasopharyngeal carcinoma observed in a non-endemic population[J].Radiother Oncol, 2009,92(1): 105-10. |
| [2] | Lu H, Peng L, Yuan X, et al. Concurrent chemoradiotherapy in locally advanced nasopharyngeal carcinoma: a treatment paradigm also applicable to patients in Southeast Asia[J]. Cancer Treat Rev, 2009, 35(4): 345-53. |
| [3] | Chan AT, Leung SF, Ngan RK, et al. Overall survival after concurrent cisplatin- radiotherapy compared with radiotherapy alone in local regionally advanced nasopharyngeal carcinoma[J].J Nati Cancer Inst,2005,97(7):536-9. |
| [4] | Lin JC, Jan JS, Hsu CY, et al. Outpatient weekly chemotherapy in patients with nasopharyngeal carcinoma and distant metastasis [J]. Cancer, 1998,83(4):635-40. |
| [5] | Yang ES, Murphy BM, Chung CH, et al. Evolution of clinical trials in head and neck cancer[J].Crit Rev Oncol Hematol, 2009,71(1):29-42. |
| [6] | Zhang L,Zhang Y,Huang PY,et al. Phase II clinical study of gemcitabine in the treatment of patients with advanced nasopharyngeal carcinoma after the failure of platinum-based chemotherapy[J]. Cancer Chemother Pharmacol,2008, 61(1):33-8. |
| [7] | Chi KH, Chang YC, Chan WK, et al. A Phase II study of carboplatin in nasopharyngeal carcinoma[J].Oncology, 1997,54(3):203-7. |
| [8] | Tan EH, Khoo KS, Wee J, et al. Phase II trial of a paclitaxel and carboplatin combination in Asian patients with metastatic nasopharyngeal carcinoma[J]. Ann Oncol, 1999,10(2):235-7. |
| [9] | Ma BB, Tannock IF, Pond GR,et al. Chemotherapy with gemcitabine-containing regimens for locally recurrent or metastaticnasopharyngealcarcinoma[J]. Cancer, 2002,95(12):2516-23. |
| [10] | Edge S, Byrd DR, Compton CC,et al. AJCC Cancer Staging Manual[S]. 7th ed. New York: Springer, 2010. |
| [11] | International Commission on Radiation Units and Measurements. Prescribing, recording, and reporting photon beam therapy (Suppl ement to ICRU report 50 ) [J]. Bethesda: ICRU, 1999. |
| [12] | Mao YP, Li WF, Chen L,et al. A clinical verification of the Chinese 2008 staging system for nasopharyngeal carcinoma[J]. Ai Zheng, 2009,28(10):1022-8. [毛燕萍,李文斐,陈磊,等.鼻咽癌2008分期的临床验证[J].癌症,2009,28(10):1022-8.] |
| [13] | Eisenhauer EA, Therasse P, Bogaerts J,et al. New response evaluation criteria in solid tumours: revised RECIST guideline (version1.1) [J]. Eur J Cancer, 2009, 45(2):228-47. |
| [14] | Siu LL, Czaykowski PM, Tannock IF. Phase I/II study of the CAPABLE regimen for patients with poorly differentiated carcinoma of the nasopharynx[J]. J Clin Oncol, 1998,16(7): 2514-21. |
| [15] | Hasbini A, Mahjoubi R, Fandi A,et al. Phase Ⅱ trial combining mitomycin with 5-fluorouracil, epirubicin, and cisplatin in recurrent and metastatic undifferentiated carcinoma of the nasopharyngeal type[J]. Ann Oncol, 1999,10(4):421-5. |
| [16] | Taamma A, Fandi A, Azli N, et al. Phase Ⅱ trial of chemotherapy with 5-fluorouracil, bleomycin, epirubicin, and cisplatin for patients with locally advanced, metastatic, or recurrent undifferentiated carcinoma of the nasopharyngeal type[J]. Cancer, 1999, 86(7):1101-8. |
| [17] | Leong SS,Wee J,Rajan S,et al.Triplet combination of gemcitabine, paclitaxel, and carboplatin followed by maintenance 5-fluorouracil and folinic acid in patients with metastatic nasopharyngeal carcinoma[J]. Cancer, 2008, 113(6):1332-7. |
| [18] | Yu JP, Sun SP, Ni XC, et al. Effectiveness and safety of paclitaxel liposomes plus cisplatin combined with radiotherapy for malignant tumors[J]. Ai Zheng Jin Zhan, 2010,8(2): 180-2,188. [于静萍, 孙 苏平, 倪新初,等. 紫杉醇脂质体加顺铂联合放疗治疗恶性肿瘤的疗效和安全性研究[J].癌症进展,2010,8(2): 180-2,188.] |
| [19] | Chen L,Zhuang ZX,Tao JL,et al.Efficacy and safety of weekly liposome-paclitaxel combined with tegafur on metastatic gastric cancer[J].Zhong Liu Fang Zhi Yan Jiu,2013,40(5):478-80.[ 陈蕾, 庄志祥,陶家龙,等.每周脂质体紫杉醇联合替吉奥胶囊治疗晚期胃癌的临床疗效及安全性[J].肿瘤防治研究,2013,40(5):478-80.] |
| [20] | Chitapanarux I, Lorvidhaya V, Kamnerdsupaphon P,et al. Chemora diation comparing cisplatin versus carboplatin in locally advanced nasopharyngeal cancer: randomised, non-inferiority, open trial[J]. Eur J Cancer, 2007, 43(9):1399-406. |
 2014, Vol. 41
2014, Vol. 41