文章信息
- 陈晓秋,刘楠楠,王树滨. 2014.
- CHEN Xiaoqiu, LIU Nannan, WANG Shubin. 2014.
- 晚期胃癌维持化疗的生存分析
- Survival of Advanced Gastric Cancer Patients Treated with Maintenance Chemotherapy
- 肿瘤防治研究, 2014, 41(12): 1339-1342
- Cancer Research on Prevention and Treatment, 2014, 41(12): 1339-1342
- http://www.zlfzyj.com/CN/10.3971/j.issn.1000-8578.2014.12.019
-
文章历史
- 收稿日期:2013-11-06
- 修回日期:2014-04-16
胃癌是全球发病率较高的恶性肿瘤之一,在全球因胃癌死亡的患者中,中国占50%,它较低 的早诊率使得临床工作中晚期患者更为多见,如 何延长患者的生存期并提高生活质量成为治疗重 点之一。恶性肿瘤的维持治疗是指患者接受一定 疗程化疗达到最大肿瘤控制效应后再接受药物治 疗,以取得最大的肿瘤缓解与生存[1],关于维持治疗,在非小细胞肺癌中的研究相对成熟[2, 3],近年 来在晚期乳腺癌以及结直肠癌中也陆续开展了相 关临床试验,并得到了阳性结果[4, 5]。基于此,我 们观察以有效低毒的化疗药物卡陪他滨在晚期胃 癌患者中进行一线化疗后的维持治疗是否可改善 患者生存、影响预后。
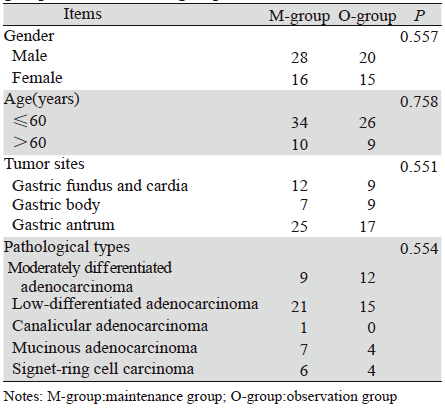
1 资料与方法 1.1 临床资料入选2006年8月—2011年8月于北京大学深圳医 院肿瘤科行一线化疗的晚期胃癌患者102例,均经 病理学证实,排除合并其他恶性肿瘤,既往未接 受过放化疗,血常规、心、肺、肝、肾功能检查 正常,无脑及周围神经系统疾病,影像学检查均 有可测量病灶,KPS评分≥60,ECOG≤2,预计 生存期≥3月,全组患者均接受一线化疗,达疾病 控制(包括完全缓解、部分缓解、疾病稳定)者 共79例(遵照患者意愿分为维持组及观察组), 其中男性48例,女性31例,年龄26~75岁,中位年 龄52岁;胃底贲门癌21例,胃体癌16例,胃窦癌 42例;中分化腺癌21例,低分化腺癌36例,管状 腺癌1例,黏液腺癌11例,印戒细胞癌10例。两组 患者性别、年龄、肿瘤部位、病理类型均具有可 比性(P>0.05),见表 1。
 |
化疗前进行全面的影像学检查作为基线检 查。一线化疗方案包括:XELOX方案(奥沙利铂 130 mg/m2静脉滴注d1+卡培他滨1.0 g/m2口服,2次 /日,d1~14,3周重复),FOLFOX6方案(奥沙利铂85 mg/m2静脉滴注d1+亚叶酸钙0.4 g/m2静脉滴 注d1+5-氟尿嘧啶0.4 g/m2静脉推注 d1+5-氟尿嘧啶 2.4 g/m2持续静脉滴注46~48 h,d1,2周重复)。 XELOX方案4~6周期、FOLFOX6方案6~8周期,期 间出现疾病进展患者进入二线化疗,达疾病控制 患者分别进入维持组或观察组,维持组以卡培他 滨单药化疗(1.0 g/m2口服,2次/日,d1~14,3周 重复)直至疾病进展或出现不可耐受的毒性,观 察组单纯随访。 1.3 不良反应评定、疗效评价及随访
化疗不良反应采用NCI-CTC v3.0进行评估, 其中神经毒性按奥沙利铂Levi专用感觉神经1.3毒 性分级标准评定。随访期间维持组每3周期、观 察组每2月进行影像学检查评价疗效,疗效评价 按RECIST标准分为完全缓解(CR)、部分缓解 (PR)、疾病稳定(SD)、疾病进展(PD)。 1.4 统计学方法
应用SPSS13.0软件进行统计学分析,χ2检验比 较两组一般临床资料,非参数检验比较两组的疗 效及不良反应,Kaplan-Meier乘积极限法计算中位 生存期、绘制生存曲线,组间差异采用Log rank检 验,P<0.05为差异有统计学意义。 2 结果 2.1 一线化疗疗效
102例患者经一线化疗后CR 3例、PR 39例、 SD 37例、PD 23例,客观缓解率41.2%,疾病控 制率77.5%;达到疾病控制患者共79例,其中2例 CR、23例PR、19例SD进入维持组,1例CR、16例 PR、18例SD进入观察组。
2.2 维持化疗进行情况一线化疗结束后的随访期间,维持组1例CR仍 维持CR,1例PR进一步好转为CR,1例PR进一步 缩小,但未达CR,1例PR仍维持PR,余均PD;观 察组1例CR仍CR,余均PD,两组客观有效率差异 无统计学意义(P>0.05)。
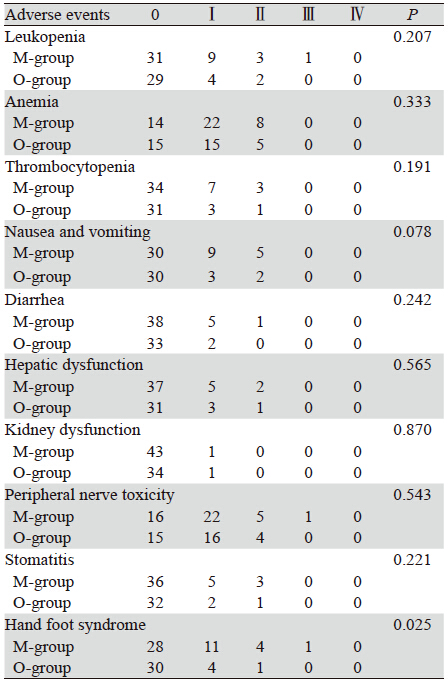
2.3 维持组与观察组不良反应比较卡陪他滨维持组手足综合征的发生率明 显高于单纯观察组,分别为36.4%、14.3%(P <0.05),其中,仅1例维持组患者出现Ⅲ度手足 综合征,予减量25%后再维持治疗2周期,期间再 度出现Ⅲ度反应,后停止治疗,4例Ⅱ度手足综合 征患者予减量25%后均缓解;恶心呕吐在维持组略 高,但差异无统计学意义(P=0.078);两组在白 细胞减少、贫血、血小板减少、腹泻、肝功能异常、肾功能损害、外周神经毒性、口腔炎等方面 差异均无统计学意义(P>0.05),见表 2,随访期 间不良反应多数为Ⅰ~Ⅱ度,偶见Ⅲ度,未见Ⅳ度 反应发生。
 |
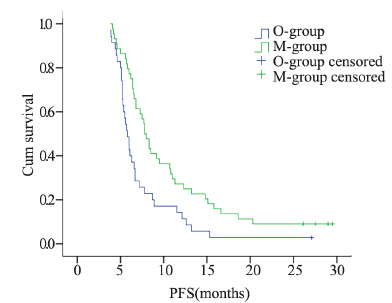
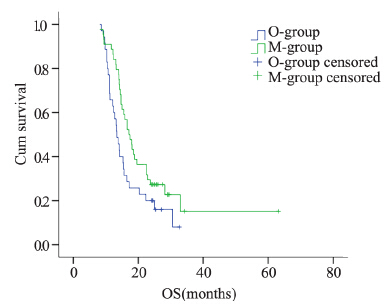
随访截至2013年8月,随访率100%。维持组 中位无进展生存时间(mPFS)为7.8月(95%CI: 6.9~8.7),较观察组的5.8月(95%CI: 5.2~6.4) 有所延长(P=0.005),两组患者的无进展生存 曲线见图 1;维持组中位总生存时间(mOS) 为17.1月(95%CI: 14.7~19.5),观察组13.4月 (95%CI: 11.8~15.0),两组比较差异有统计学意 义(P=0.041),两组患者的总生存曲线见图 2。
|
| 图 1 维持治疗组和观察组晚期胃癌患者无进展生存曲线 Figure 1 Progression free survival curves of maintenance group and observation group |
|
| 图 2 维持治疗组和观察组患者总生存曲线 Figure 2 Overall survival curves of maintenance group and observation group |
晚期胃癌的5年生存率不足10%,迄今为止 除TOGA试验证实了赫赛汀在晚期胃癌中的作用, 其他关于靶向药物的临床试验结果均为阴性,故 化疗仍是晚期胃癌综合治疗的核心。与最佳支持治疗相比,联合化疗可以改善患者的生存质量以 及总生存率[6, 7],但持续的联合化疗常常产生累 积性毒性,如骨髓抑制、神经毒性等,使得患者 耐受性下降,也限制了部分有效药物的应用。维 持治疗是一种新的治疗模式,即完成一定的化疗 周期达到疾病控制效应后,进行低强度化疗和 (或)靶向治疗来控制肿瘤,它将治疗时间最大 化,并保存了患者后期接受进一步联合治疗的能 力,降低了累积毒性的产生、保留了有效药物的 后继应用,理想的维持治疗药物应具备有效、耐 受性好、使用方便的特点。维持治疗较成功的典 范是在晚期非小细胞肺癌的研究中,单药化疗如 培美曲塞[2]能够延长患者的无进展生存期和总生存 期,近期的一项大规模多中心临床研究[3]进一步证 实吉非替尼可以延长晚期非小细胞肺癌患者的无 进展生存期。此外,在晚期乳腺癌和结直肠癌的 维持治疗研究中也得到类似结果[4, 5]。但在晚期胃 癌中维持治疗的研究相对罕见。
氟尿嘧啶类加奥沙利铂是晚期胃癌标准的一 线治疗方案之一,本研究采用XELOX及FOLFOX6 方案对102例晚期初治的胃癌患者进行化疗,结果 显示总体客观缓解率41.2%、疾病控制率77.5%, 与报道相似[8, 9]。卡培他滨是一种口服氟尿嘧啶类 药物,它能在肿瘤细胞内高水平的胸苷磷酸化酶 的作用下转化为5-Fu从而发挥抗肿瘤作用,具有 使用方便、不良反应小的特点,有研究显示其单 药治疗晚期胃癌有效率达34%[10],故以卡培他滨进 行维持治疗是一种较好的选择。
本研究采用卡培他滨进行维持治疗,结果显 示,维持组44例患者截至随访结束有4例仍维持 疗效,而观察组39例仅1例未进展,但两组客观有 效率比较差异无统计学意义(P=0.170),考虑与 本研究从开始到随访结束历时较长时间相关(7 年)。生存分析结果显示,维持组中位无进展生 存时间8.0月,观察组6.0月,两组比较差异有统计 学意义(P<0.05),维持组中位总生存时间16.6 月,较观察组13.8月亦有所延长(P=0.046), 即卡培他滨维持化疗可以延长晚期胃癌患者的无 进展生存期和总生存期。比较两组不良反应情 况,维持组在手足综合征的发生上高于观察组 (P<0.05),但只1例患者因两次的Ⅲ度反应而 停药,Ⅱ度患者经减量、Ⅰ度患者继续原剂量均 可耐受;其他不良反应,包括骨髓抑制、恶心呕 吐、腹泻、肝肾功能异常、外周神经毒性、口腔 炎等两组差异均无统计学意义(P>0.05),即患 者对维持治疗耐受性较好。
本研究显示,氟尿嘧啶类/奥沙利铂方案一线 化疗达疾病控制后以卡培他滨维持治疗可使晚期 胃癌患者获益,表现为无进展生存期和总生存期 的改善,且不良反应较小,患者耐受性良好,可 考虑临床开展应用。因本研究例数尚少,故仍需 更大规模的临床试验进一步予以证实。
| [1] | Paz-Ares LG, Altug S, Vaury AT, et al. Treatment rationale and study design for a phaseⅢ, double-blind, placebo-controlled study of maintenance pemetrexed plus best supportive care versus best supportive care immediately following induction treatment with pemetrexed plus cisplatin for advanced non-squamous non-smallcell lung cancer[J]. BMC Cancer, 2010, 10: 85. |
| [2] | Ciuleanu T, Brodowicz T, Zielinski C, et al. Maintenance pemetrexed plus best supportive care versus placebo plus best supportive care for non-small-cell lung cancer: a randomized, doubleblind, phase 3 study[J]. Lancet, 2009, 374(9699): 1432-40. |
| [3] | Zhang L, Ma S, Song X, et al. Gefitinib versus placebo as maintenance therapy in patients with locally advanced or metastatic non-small-cell lung cancer(INFORM; C-TONG 0804): a multicentre, double-blind randomized phrase 3 trial[J]. Lancet Oncol, 2012,13(5):466-75. |
| [4] | Huang H, Jiang Z, Wang T, et al. Single-agent capecitabine maintenance therapy after response to capecitabine-based combination chemotherapy in patients with metastatic breast cancer[J]. Anticancer Drugs, 2012,23(7):718-23. |
| [5] | Chibaudel B, Maindrault-Goebel F, Lledo G, et al. Can chemotherapy be discontinued in unresectable metastatic colorectal cancer? The GERCOR OPTIMOX2 study[J]. J Clin Oncol, 2009, 27(34): 5727-33. |
| [6] | Wanmer AD, Unverzagt S, Grothe W, et al. Chemotherapy for advanced gastric cancer[J]. Cochrane Database Syst Rev, 2010, 17 (3): CD004064. |
| [7] | Pyrh?nen S, Kuitunen T, Nyandoto P, et al. Randomised comparison of fluorouracil, epidoxorubicin and methotrexate(FEMTX) plus supportive care with supportive care alone in patients with nonresectable gastric cancer[J]. Br J Cancer, 1995, 71(3):587-91. |
| [8] | Zhang R, Yan H, Wang M, et al. A meta-analysis on the effects of regimen XELOX versus FOLFOXs for treatment of Chinese patients with metastatic gastric cancer[J]. J Cap Med Univ, 2013, 34(3): 422-7. |
| [9] | Liu C, Sun Q, Hang X, et al. Multicenter phase Ⅱ study of capectabine plus oxaliplatin as a first-line therapy in Chinese patients with advanced gastric cancer[J]. Anticancer Drugs, 2008, 19(8):825-31. |
| [10] | Hong YS, Song SY, Lee SI, et al. A phase Ⅱ trial of capecitabine in previously untreated patients with advanced and/or metastatic gastric cancer [J]. Ann Oncol, 2004, 15(9): 1344-7. |
 2014, Vol. 41
2014, Vol. 41


