文章信息
- 王俊斌,吴穷,邹维艳,汪子书,杨燕,郑荣生. 2014.
- WANG Junbin, WU Qiong, ZOU Weiyan, WANG Zishu, YANG Yan, ZHENG Rongsheng. 2014.
- 雷替曲塞或氟尿嘧啶联合伊立替康二线治疗晚期结直肠癌疗效分析
- Therapeutic Effect of Raltitrexed or Fluorouracil plus Irinotecan as Second-line Treatment for Advanced Colorectal Cancer
- 肿瘤防治研究, 2014, 41(12): 1335-1338
- Cancer Research on Prevention and Treatment, 2014, 41(12): 1335-1338
- http://www.zlfzyj.com/CN/10.3971/j.issn.1000-8578.2014.12.018
-
文章历史
- 收稿日期:2013-11-25
- 修回日期:2014-02-26
2.233000 蚌埠,蚌埠医学院组胚教研室
结直肠癌是最常见的恶性肿瘤之一,近年 来,随着人们生活方式的改变,结直肠癌的发病 率及死亡率呈上升趋势。尽管手术是治疗的主要 手段,但仍有部分患者术后出现复发和转移,且 约20%~25%的患者初诊时即已发生转移,手术无 法根治病情,化疗是晚期结直肠癌的主要治疗手 段。过去40年,氟尿嘧啶(fluorouracil,5-Fu) 一直是治疗晚期结直肠癌最常用的化疗药物,以 5-Fu为基础的方案一线治疗晚期结直肠癌,二线 治疗仍使用5-Fu联合化疗,治疗效果不甚满意, 另外由于持续输注,易增加口腔黏膜炎、感染等 风险,影响患者生活质量[1, 2]。因此,一线使用 以5-Fu为基础方案治疗失败后二线治疗寻找替代 5-Fu的药物显得尤为重要。雷替曲塞(raltitrexed) 是一种新型的抑制胸腺嘧啶合成酶活性的抗叶酸 制剂,对晚期结直肠癌治疗的疗效已被证实,与 5-Fu相比,雷替曲塞具有更强的抗人结肠癌肿瘤细 胞的活性,毒性小、活性高、使用方便等特点[3, 4]。 目前晚期结直肠癌一线化疗失败后尚无有效的 二线方案,我们应用雷替曲塞或5-Fu/亚叶酸钙(leucovorin,LV) 联合伊立替康(Irinotecan,CPT-11) 方案治疗晚期结直肠癌52例,对其疗效及不良反 应进行分析,结果报道如下。
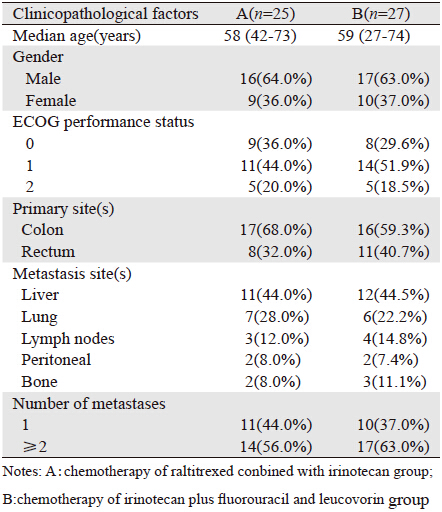
1 资料与方法 1.1 一般资料选取2011年7月—2013年8月在蚌埠医学院第 一附属医院住院治疗的晚期及复发转移性结直 肠癌52例。A组25例:男性16例,女性9例;年 龄42~73岁,中位年龄61岁;结肠癌17例,直肠 癌8例。B组27例:男性17例,女性10例;年龄 27~74岁,中位年龄62岁;结肠癌16例,直肠癌11 例。所有患者均有明确的病理组织学或细胞学诊 断;两组患者均使用FOLFOX(包括FOLFOX4, mFOLFOX6)一线方案化疗后病情进展;既往均 未使用过雷替曲塞治疗;ECOG评分:0~2分;年 龄18~75岁;至少有一个CT或MRI可测量的客观 靶病灶;预计生存期均超过3月;血常规及肝肾 功能基本正常,无化疗禁忌证;无长期慢性腹泻 病史及肠梗阻史;并能随访。两组患者年龄、转 移部位及数目等临床特征比较差异无统计学意义 (P>0.05),见表 1。
 |
A组:采用雷替曲塞联合伊立替康化疗。雷 替曲塞2.5 mg/m2,静脉滴注15 min,第1天(在伊 立替康后2 h使用);伊立替康180 mg/m2,静脉 滴注90 min,第1天;14天为1周期。B组:采用 伊立替康联合氟尿嘧啶及亚叶酸钙化疗。伊立替 康160~180 mg/m2,静脉滴注90 min,d1,CF 200 mg/ m2,静脉滴注2 h,d1~d2;5-Fu 400 mg/m2,静脉推 注,4~10 min,d1~d2;5-Fu 1 200 mg/m2,持续泵 入维持44 h,14天为1周期。如果两组化疗中出现 Ⅳ度骨髓抑制和(或)胃肠道反应,化疗药物剂量 减少20%。所有患者在化疗前30 min均给予昂丹司 琼预防性止吐处理。两组均每3周期评价疗效1次, 直至病情进展或不能耐受,每组最多化疗12周期。 1.3 疗效评价标准 1.3.1 临床疗效的评价
每组在完成3周期后进 行疗效评价,根据 RECIST1.0版实体瘤疗效评价 标准分为完全缓解(CR)、部分缓解(PR)、 病情稳定(SD)和病情进展(PD),以CR+PR 为有效率(RR),以CR+PR+SD为疾病控制率 (DCR),两组均在完成3个周期治疗之后进行首 次疗效评价,如疗效评价为CR、PR和SD者,均 可继续原方案治疗,其中,CR和PR患者于4周后 重新进行疗效确认,疗效评价为PD者,则终止治 疗。疾病进展时间(time to disease progression, TTP)为化疗开始至出现疾病进展的时间,疗效确 认为CR、PR和SD者,每1~2个月随访一次,直至 病情进展,总结TTP。 1.3.2 不良反应的评价
每周期化疗均观察不良反应情况,按照 (NCI-CTC)3.0版进行分级,分为Ⅰ~Ⅳ度。主要 观察指标:RR和TTP。
1.4 统计学方法采用SPSS16.0软件进行统计分析,计数资料 比较采用χ2检验,生存分析情况采用Kaplan-Meier 法,以P﹤0.05为差异有统计学意义。
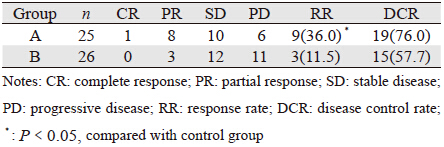
2 结果 2.1 近期疗效A组共完成164周期化疗,B组共完成171周期 化疗,B组中有1例患者出现Ⅳ度腹泻退出治疗, 不纳入疗效评价,但纳入不良反应评估。A组CR 1例,PR 8例,SD 10例,PD 6例;B组无CR病 例,PR 3例,SD 12例,PD 11例。两组RR分别为 36.0%和11.5%,差异有统计学意义(χ2=4.238, P=0.040),DCR分别为76.0%和57.7%,差异无统 计学意义(χ2=1.922,P=0.166),见表 2。
 |
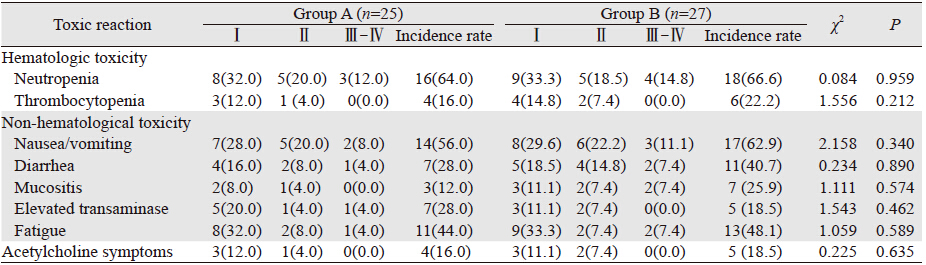
两组治疗的主要不良反应是中性粒细胞减 少、乏力和胃肠道反应,大多为Ⅰ~Ⅱ度。特有的 不良反应主要是延迟性腹泻,多为Ⅰ~Ⅱ度,Ⅲ度 以上腹泻发生率低,经规范使用易蒙停解救治疗 后,能在短时间内控制症状,B组有1例患者因Ⅳ 度腹泻退出治疗,A组黏膜炎的发生率较B组低, 但两组不良反应的发生率比较差异无统计学意义 (P﹥0.05),无治疗引起相关性死亡,见表 3。
 |
截至2013年8月31日,初步随访显示,A组 中位TTP为6.0月(2.9~10.5月);B组中位TTP 为4.5月(1.5~9.0月)。Kaplan-Meier生存分析A 组中位TTP较B组长1.5月,但差异无统计学意义 (χ2=12.883,P=0.978)。 3 讨论
目前结直肠癌发病率呈上升趋势,复发和转移 是其主要死亡原因,以化疗为主的综合治疗仍然是 晚期结直肠癌的主要治疗手段。研究显示,化疗可 使晚期结直肠癌患者的生存期延长至2年。5-Fu是 晚期结直肠癌治疗的基本化疗药物[5],其通过抑制 胸苷酸合成酶来阻碍DNA合成,抑制肿瘤细胞生 长。晚期结直肠癌一直采用以5-Fu或其类似物为 基础的化疗方案,近期报道的以5-Fu为主的联合 化疗一线治疗晚期结直肠癌,其有效率近50%[6]。 但晚期结直肠癌患者一线化疗失败后大部分继续进行二线化疗,以CPT-11为主的FOLFIRI方案作 为一线FOLFOX方案失败后的二线方案,其有效 率仅为4%~10%,PFS为2.6~3.9月[7, 8]。临床上, 5-Fu通常通过连续静脉输注或经外周穿刺中心静 脉置管术(PICC)置管后持续泵入的方式给药, 易增加静脉炎、血栓及感染等风险,并需定期行 PICC护理,5-Fu的使用还需要亚叶酸钙增敏,增 敏后提高疗效的同时也增加了不良反应,影响患 者生活质量,另外部分患者因体内二氢嘧啶脱氢 酶的缺乏引起氟尿嘧啶蓄积更易导致严重不良反 应的发生。另有研究表明,一线使用5-Fu治疗进 展后,二线继续以5-Fu为基础的联合方案治疗并 不能提高疗效,认为二线无需再用5-Fu治疗[1]。因 此,寻找替代5-Fu二线治疗晚期结直肠癌药物成 为临床关注的热点。
雷替曲塞是一种新型的特异性的胸腺嘧啶合 成酶抑制剂,为喹唑啉叶酸盐类似物,其作用机 制是在体内被细胞主动摄取后很快被叶酸基聚谷 氨酸合成酶代谢为一系列多聚谷氨酸类化合物, 这些代谢物比雷替曲塞具有更强的抑制胸苷酸合 成酶作用,从而抑制肿瘤细胞DNA合成,且能长 时间潴留在细胞内发挥细胞毒作用[9, 10]。与5-Fu 相比,雷替曲塞具有更强的抗人结肠癌肿瘤细胞 的活性,无需增敏剂,研究结果显示两药的疗效 相当,雷替曲塞不良反应轻,具有使用方便、简 单,活性高等特点,对晚期结直肠癌的疗效已被 证实[3]。体外实验表明,雷替曲塞与CPT-11具有 不同的抗肿瘤机制,却具有协同抗肿瘤作用。 CPT-11是典型的拓扑异构酶Ⅰ(Topo-Ⅰ)抑制 剂,其在体内的活性代谢产物是SN-38,SN-38通 过与DNA-Topo-Ⅰ复合体的稳定结合后引起DNA 单链破坏,使DNA产生不可逆性损伤,导致细胞 死亡[11]。 CPT-11对5-Fu耐药的晚期结直肠癌患者 治疗有效率为15%~25%,一项Ⅱ期研究报道[12],雷替曲塞联合CPT-11治疗晚期结直肠癌,结果显 示 CR 3例,PR 10例,RR为27%,DCR为56.2%, mPFS为5月,不良反应可耐受。李智强等[13]报道 的雷替曲塞联合CPT-11对比FOLFIRI方案治疗晚期 结直肠癌结果显示,其RR分别为40%和13%。本 研究比较雷替曲塞联合CPT-11与CPT-11联合5-Fu 及亚叶酸钙治疗晚期结直肠癌的临床效果和不良 反应,发现A组和B组RR分别为36%和11.5%,差 异有统计学意义,DCR分别为76.0%和57.7%,差 异无统计学意义。A组和B组中位TTP分别为6.0月 和4.5月,差异无统计学意义。与国内外文献报道 相似,但由于样本量偏少,有待于扩大样本进一 步研究以探讨该方案的疗效。
CPT-11的主要不良反应是中性粒细胞减少和 延迟性腹泻,表现为剂量限制性毒性,其严重程 度与SN-38的量有关。有研究指出雷替曲塞可能减 轻CPT-11的不良反应[3]。5-Fu除主要表现胃肠道反 应外,长期使用会增加心脏毒性的风险,而雷替 曲塞心脏毒性小,在有心脏疾病患者雷替曲塞可 以替代5-Fu[14]。本研究中A组与雷替曲塞相关的不 良反应主要为中性粒细胞减少和胃肠道反应,但 多为Ⅰ~Ⅱ度,Ⅲ~Ⅳ度不良反应发生率低,与B 组比较差异无统计学意义,但口腔黏膜炎的发生 率较B组低,有无症状性肝转氨酶升高,经对症处 理后能够缓解,说明雷替曲塞临床使用安全,另 外只需15 min快速滴注,无需增敏,无需PICC置 管,使用方便,可提高患者生活质量。但目前价 格偏贵,部分患者使用受限。
大部分晚期结直肠癌患者体质较差,选择低 毒、高效的化疗方案往往能使患者真正从治疗中 获益。本研究显示雷替曲塞联合伊立替康二线 治疗晚期结直肠癌疗效肯定,不良反应可耐受 且用药方便,值得临床上对晚期结直肠癌一线 FOLFOX方案治疗失败后推荐使用。
| [1] | Seymour MT, Maughan TS, Ledermann JA, et al. Different strategies of sequential and combination chemotherapy for patients with poor prognosis advanced colorectal cancer (MRC FOCUS): a randomised controlled trial[J]. Lancet, 2007, 370(9582): 143-52. |
| [2] | Qin JL, Lu YK, Liu S, et al. Meta-analysis of the efficacy and safety of raltitrexed versus 5-fluorouracil in advanced colorectal cancer first-line chemotherapy[J]. Zhongguo Xian Dai Yi Xue Za Zhi, 2013, 23(14):84-90.[覃金莲,陆永奎,刘莎,等. 雷替曲塞对比5-氟尿嘧啶一线治疗晚期结直肠癌疗效和不良反应的Meta分析[J]. 中国现代医学杂志, 2013, 23(14): 84-90.] |
| [3] | Ying HC, YE Z. The progression of exploratory development of raltitrexed in colorectal cancer[J]. Xian Dai Zhong Liu Yi Xue, 2012, 20(6): 1318-20.[应怀昌,叶舟. 雷替曲塞在晚期结直肠癌中的应用研究进展[J]. 现代肿瘤医学, 2012, 20(6): 1318-20.] |
| [4] | Wu JB, Wang HJ, Wang SJ, et al. Comparison of Raltitrexed plus oxaliplatinl and 5-Fluorouracil/Leucovorin plus Oxaliplatinl in treatment of advanced colorectal carcinoma[J].Zhong Liu Fang Zhi Yan Jiu, 2007, 34(9):711-3.[吴建兵,王汉姣,王顺金,等.雷替曲塞联合L-OHP与5-Fu/LV联合L-OHP方案治疗晚期结直肠癌的临床疗效比较[J].肿瘤防治研究, 2007, 34(9):711-3.] |
| [5] | Grávalos C, García-Escobar I, García-Alfonso P, et al. Adjuvant chemotherapy stages Ⅱ, Ⅲ and Ⅳ of colon cancer[J]. Clin Transl Oncol, 2009, 11(8):526-33. |
| [6] | Gallagher DJ,Kemeny N.Metastatic colorectal cancer: from improved survival to potential cure[J]. Oncology, 2010, 78(3-4): 237-48. |
| [7] | Sobrero AF, Maurel J, Fehrenbacher L, et al. EPIC: Phase Ⅲ trial of cetuximab plus irinotecan after fluoropyrimidine and oxaliplatin failure in patients with metastatic colorectal cancer[J]. J Clin Oncol, 2008, 26(14):2311-9. |
| [8] | Peeters M, Price TJ, Cervantes A, et al. Randomized phase Ⅲ study of panitumumab with fluorouracil, leucovorin, and irinotecan(FOLFIRI) compared with FOLFIRI alone as secondline treatment in patients with metastatic colorectal cancer[J]. J Clin Oncol, 2010, 28(31):4706-13. |
| [9] | Jarmulaa A. Antifolate inhibitors of thymidylate synthase as anticancer drugs[J]. Mini Rev Med Chem,2010,10(13):1211-22. |
| [10] | Hagner N, Joerger M. Cancer chemotherapy: targeting folic acid synthesis[J]. Cancer Manag Res, 2010, 2: 293-301. |
| [11] | Masi G, Falcone A, Di Paolo A, et al. A phase Ⅰ and pharmacokinetic study of irinotecan given as a 7-day continuous infusion in metastatic colorectal cancer patients pretreated with 5-fluorouracil or raltitrexed[J]. Clin Cancer Res, 2004, 10:1657-63. |
| [12] | Chiara S, Nobile MT, Tomasello L, et al. Phase Ⅱ Trial of irinotecan and raltitrexed in chemotherapy-naive advanced colorectal cancer[J]. Anticancer Res, 2005, 25(2B): 1391-6. |
| [13] | Li ZQ, Wang XL. Clinical observation of raltitrexed plus irinotecan as second-line treatment in 25 patients diagnosed as advanced colorectal cancer[J]. Shi Yong Ai Zheng Za Zhi, 2012, 27(4):412-3.[李智强,王小龙. 伊立替康联合雷替曲塞二线治疗25例晚期大肠癌临床观察[J]. 实用癌症杂志,2012, 27(4): 412-3.] |
| [14] | Kelly C, Bhuva N, Harrison M, et al. Use of raltitrexed as analternative to 5-fluorouracil and capecitabine in cancer patients with cardiac history[J]. Eur J Cancer, 2013, 49(10): 2303-10. |
 2014, Vol. 41
2014, Vol. 41


